题目内容
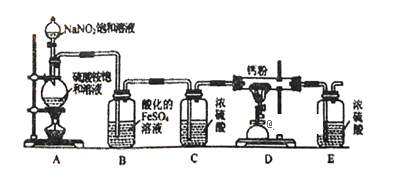
【题目】(1)气态三氧化硫以单分子形式存在,其分子的立体构型为________形,从电子云重叠方式看共价键的类型有________种;固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为________。
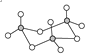
(2)某FexNy的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n)CunNy。FexNy转化为两种Cu替代型产物的能量变化如图2所示,其中更稳定的Cu替代型产物的化学式为__。
图1 FexNy晶胞结构示意图 图2转化过程的能量变化
图2转化过程的能量变化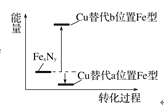
(3)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为a=0.446 nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为__ nm,与K紧邻的O个数为____。
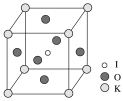
(4)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于_______位置,O处于______位置。
【答案】平面三角 2 sp3 Fe3CuN 0.315 (或 ![]() ×0.446) 12 体心 棱心
×0.446) 12 体心 棱心
【解析】
(1) SO3中S原子价层电子对数=3+![]() =3,且不含孤电子对,根据价层电子对互斥理论判断其空间构型;该分子中S-O原子之间存在共价键;该分子中每个S原子价层电子对数都是4,根据价层电子对互斥理论判断S原子杂化类型;
=3,且不含孤电子对,根据价层电子对互斥理论判断其空间构型;该分子中S-O原子之间存在共价键;该分子中每个S原子价层电子对数都是4,根据价层电子对互斥理论判断S原子杂化类型;
(2) 能量越低越稳定,故Cu替代a位置的Fe形成的物质更稳定,形成晶胞中N原子处于体心、Cu原子处于顶点、Fe原子处于面心,利用均摊法计算晶胞中各原子数目,进而确定化学式;
(3) K与O间的最短距离为面对角线的一半;O位于面心,K位于顶点,1个面心为2个晶胞共有,1个顶点为8个晶胞共有;
(4) 在KIO3晶胞结构的另一种表示中,I处于各顶角位置,个数为8×![]() =1,则K也为1,应位于体心,则O位于棱心,个数为12×
=1,则K也为1,应位于体心,则O位于棱心,个数为12×![]() =3。
=3。
(1) SO3中S原子价层电子对数=3+![]() =3,且不含孤电子对,根据价层电子对互斥理论判断其空间构型为平面正三角形;该分子中S-O原子之间存在σ和离域大π键,所以共价键类型2种;该分子中每个S原子价层电子对数都是4,根据价层电子对互斥理论判断S原子杂化类型为sp3;
=3,且不含孤电子对,根据价层电子对互斥理论判断其空间构型为平面正三角形;该分子中S-O原子之间存在σ和离域大π键,所以共价键类型2种;该分子中每个S原子价层电子对数都是4,根据价层电子对互斥理论判断S原子杂化类型为sp3;
(2) 能量越低越稳定,故Cu替代a位置的Fe形成的物质更稳定,形成晶胞中N原子处于体心、Cu原子处于顶点、Fe原子处于面心,晶胞中N原子数目=1,N(Cu)=8×![]() =1,N(Fe)=6×
=1,N(Fe)=6×![]() =3,故化学式为:Fe3CuN;
=3,故化学式为:Fe3CuN;
(3) K与O间的最短距离为面对角线的一半,则K与O间的最短距离为![]() ×0.446nm=0.315nm,O位于面心,K位于顶点,1个面心为2个晶胞共有,1个顶点为8个晶胞共有,即与K紧邻的O个数为
×0.446nm=0.315nm,O位于面心,K位于顶点,1个面心为2个晶胞共有,1个顶点为8个晶胞共有,即与K紧邻的O个数为![]() =12个;
=12个;
(4) 在KIO3晶胞结构的另一种表示中,I处于各顶角位置,个数为8×![]() =1,则K也为1个,应位于体心,则O位于棱心,每个棱为4个晶胞共有,则O个数为12×
=1,则K也为1个,应位于体心,则O位于棱心,每个棱为4个晶胞共有,则O个数为12×![]() =3。
=3。

 考前必练系列答案
考前必练系列答案【题目】验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。
① | ② | ③ |
|
|
|
在Fe表面生成蓝色沉淀 | 试管内无明显变化 | 试管内生成蓝色沉淀 |
下列说法不正确的是
A. 对比②③,可以判定Zn保护了Fe
B. 对比①②,K3[Fe(CN)6]可能将Fe氧化
C. 验证Zn保护Fe时不能用①的方法
D. 将Zn换成Cu,用①的方法可判断Fe比Cu活泼
【题目】实验室用密度为1.18g/ml,质量分数为36.5%浓盐酸配制250mL0.1mol/L的盐酸溶液,填空并请回答下列问题:
(1)配制250mL0.1mol/L的盐酸溶液
实际应量取盐酸体积/ml | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它仪器 |
______________ | ______________ | ______________ |
(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)______________;
A.用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B.用量筒量准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(3)操作A中,将洗涤液都移入容量瓶,其目的是_________________________________,溶液注入容量瓶前需恢复到室温,这是因为______________________________________;
(4)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)?若没有进行A操作_______________;若加蒸馏水时不慎超过了刻度_______________;若定容时俯视刻度线___________________。
(5)若实验过程中出现如下情况如何处理?加蒸馏水时不慎超过了刻度_______________;向容量瓶中转移溶液时(实验步骤②)不慎有液滴掉在容量瓶外面_____________________。