题目内容
【题目】(1)中国的高铁技术居于国际领先地位。
①高铁座椅内填充有聚氨酯软质泡沫。聚氨酯属于____(填字母)。
a.金属材料 b.无机非金属材料 c.有机高分子材料
②高铁信息传输系统中使用了光导纤维。光导纤维的主要成分是____(填字母)。
a.铜 b.石墨 c.二氧化硅
③高铁轨道建设需用大量水泥。生产水泥的主要原料为黏土和____(填字母)。
a.石灰石 b.粗盐 c.纯碱
(2)营养均衡有利于身体健康。
①人体内提供能量的主要营养物质为____、糖类和蛋白质。淀粉在人体内水解的最终产物是____。
②维生素是人体需要的营养物质。如图为某品牌维生素C泡腾片说明书的部分内容。该泡腾片中添加的着色剂是____,甜味剂是___。泡腾片溶于水时产生“沸腾”效果,是由于添加的酒石酸和___反应释放出了气体。

(3)煤炭在我国能源结构中占有重要地位,合理使用有利于社会可持续发展。
①控制燃煤产生的SO2排放,能够减少____型酸雨的形成。燃煤排放的烟气中还含有其他污染物,请列举一种:_____。
②燃煤产生的CO2用NH3处理可生产多种化工产品。用氨水吸收CO2可制得碳铵(NH4HCO3),写出该反应的化学方程式_____。用液氨与CO2反应可制备尿素[CO(NH2)2]。尿素和碳铵这两种氮肥中,氮元素的质量分数较高的是_____。
③煤的气化和液化是实现能源清洁化的重要途径。水煤气中CO和H2在加热、加压和催化剂存在条件下可以合成液体燃料(CH3OH),该反应的化学方程式为_____。
【答案】c c a 油脂 葡萄糖 喹啉黄 糖精钠、蔗糖 碳酸氢钠 硫酸 可吸入颗粒物等 NH3·H2O + CO2=NH4HCO3 尿素 CO +2H2 ![]() CH3OH
CH3OH
【解析】
(1)①聚氨酯泡沫,根据名称为聚合物,属于有机高分子材料;答案为c;
②光导纤维的主要成分为二氧化硅;答案为c;
③生成水泥的主要成分为石灰石、黏土;答案为a;
(2)①人体内提供能量的主要营养物质有油脂、糖类、蛋白质;淀粉属于糖类,在人体内最终水解为葡萄糖;答案为油脂 葡萄糖;
②辅料中有柠檬香精,橙味香精、喹啉黄、糖精钠、蔗糖、氯化钠、碳酸氢钠、酒石酸等。从其名称来可以判断其作用,着色剂为喹啉黄,甜味剂有蔗糖、糖精钠;溶于水产生沸腾的效果由于酒石酸和碳酸氢钠反应生成CO2;答案为喹啉黄 糖精钠、蔗糖 碳酸氢钠;
(3)①SO2溶于水后生成亚硫酸,被氧气氧化成硫酸,减少SO2的排放,可以减少硫酸型的酸雨;燃煤排放的烟气中除SO2还有煤炭未完全燃烧生成的CO,高温下氮气和氧气生成的NO,氮氧化物等,还有些烟尘,答案为可吸入颗粒物等;
②氨水吸收CO2制取碳酸铵,为酸性氧化物与碱的反应,答案为NH3·H2O + CO2=NH4HCO3。NH4HCO3中N的质量分数![]() ;CO(NH2)2中N的质量分数
;CO(NH2)2中N的质量分数![]() ,N含量较高的是尿素;
,N含量较高的是尿素;
③水煤气中CO和H2在加热、加压和催化剂存在条件下可以合成液体燃料(CH3OH),根据原子守恒,得到化学方程式为CO +2H2 ![]() CH3OH。
CH3OH。

 阅读快车系列答案
阅读快车系列答案【题目】有X、Y、Z、M、R五种短周期主族元素,部分信息如下表所示:
X | Y | Z | M | R | |
原子半径/nm | 0.074 | 0.099 | |||
主要化合价 | +4,-4 | -2 | -1,+7 | ||
其它 | 阳离子核外无电子 | 无机非金属材料的主角 | 第三周期简单离子半径最小 |
请回答下列问题:
(1)Z与NaOH溶液反应的离子方程式:___。(用元素符号表示,下同。)
(2)下列事实能说明R非金属性比Y强这一结论的是___(选填字母序号)。
a.常温下Y的单质呈固态,R的单质呈气态
b.气态氢化物稳定性R>Y
c.Y与R形成的化合物中Y呈正价
d.Y与R各自形成的含氧酸中R的氧化性更强
(3)经测定X2M2为二元弱酸,写出X2M2的电子式___。其酸性比碳酸的还要弱,请写出其第一步电离的电离方程式___。
(4)已知I2能做X2M2分解的催化剂:
第一步:X2M2+I2=2XIM;
第二步:……
请写出第二步反应的化学方程式___。
(5)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现在改用X2M2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式___。
【题目】某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。请填写下列空白:
Ⅰ.测定过氧化氢的含量
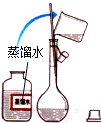
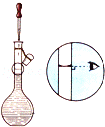
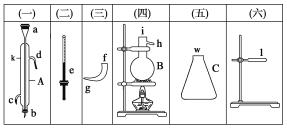
(1)移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250 mL_______(填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00 mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式为________。
(3)判断滴定到达终点的现象是_________________________。
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为____________。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________(填“偏高”或“偏低”或“不变”)。
Ⅱ.探究过氧化氢的性质
该化学兴趣小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)
请将他们的实验方法和实验现象填入下表:
实验内容 | 实验方法 | 实验现象 |
验证氧化性 | ____________ | ____________ |
验证不稳定性 | ____________ | ____________ |