题目内容
1.常温下,某CH3COONa与CH3COOH的混合溶液的pH=7,则下列离子浓度之间的关系错误的是( )| A. | c(Na+)>c(CH3COO-) | B. | c(Na+)+c(H+)=c(OH-)+c(CH3COO-) | ||
| C. | c(Na+)<c(CH3COO-) | D. | c(Na+)<c(CH3COO-)+c(OH-) |
分析 常温下,pH=7的溶液呈中性,则c(H+)=c(OH-),溶液中存在电荷守恒和物料守恒,根据电荷守恒和物料守恒分析解答.
解答 解:常温下,pH=7的溶液呈中性,则c(H+)=c(OH-),溶液中存在电荷守恒和物料守恒,根据电荷守恒得c(Na+)+c(H+)=c(OH-)+c(CH3COO-),又因为c(H+)=c(OH-),所以c(Na+)=c(CH3COO-),c(Na+)<c(CH3COO-)+c(OH-),故选AC.
点评 本题考查离子浓度大小比较,为高频考点,明确溶液中的溶质及溶液酸碱性是解本题关键,灵活运用守恒思想分析解答,题目难度不大.

练习册系列答案
相关题目
11.下列电子式书写正确的是( )
| A. | 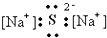 | B. |  | C. |  | D. |  |
12.下列基本操作正确的是( )
| A. | 将固体氢氧化钠用托盘天平直接称量 | |
| B. | 酒精灯的火焰必须用灯帽盖灭,不可用嘴吹灭 | |
| C. | 试管须用试管夹取用,且不能直接加热 | |
| D. | 用燃着的酒精灯去点燃另一个酒精灯 |
9.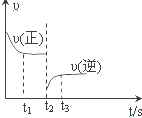 合成氨反应:N2+3H2$?_{催化剂}^{高温、高压}$2NH3 △H=-92.4kJ•mol.
合成氨反应:N2+3H2$?_{催化剂}^{高温、高压}$2NH3 △H=-92.4kJ•mol.
如图是该反应速率-时间图象,一定条件下,t1时建立平衡,t2时改变某一条件,t2时改变的条件可能是( )
 合成氨反应:N2+3H2$?_{催化剂}^{高温、高压}$2NH3 △H=-92.4kJ•mol.
合成氨反应:N2+3H2$?_{催化剂}^{高温、高压}$2NH3 △H=-92.4kJ•mol.如图是该反应速率-时间图象,一定条件下,t1时建立平衡,t2时改变某一条件,t2时改变的条件可能是( )
| A. | 升高温度 | B. | 分离出部分氨气 | C. | 降低压强 | D. | 增大反应物浓度 |
16.下列各组数据关系中,前者比后者的大是( )
| A. | 纯水100℃和25℃的pH值 | |
| B. | Na2CO3溶液中HCO3-和OH-数目 | |
| C. | 100mL0.1mol/L的CH3COOH溶液与10mL1.0mol/L的CH3COOH溶液中H+数目 | |
| D. | 同温下pH=11的KOH与pH=3的CH3COOH溶液中由水电离出的OH-离子浓度 |
6.用惰性电极电解KCl和CuSO4混合液250mL,经过一段时间后,两极均得到16.8L气体(标准状况),则下列有关描述中,正确的是( )
| A. | 阳极发生的反应只有:2Cl--2e-═Cl2↑ | |
| B. | 两极得到的气体均为混合气体 | |
| C. | 若Cu2+起始浓度为l mol•L-l,则C1-起始浓度为2 mol•L-1 | |
| D. | Cu2+的起始物质的量应小于0.75 mol |
13.能用来鉴别乙醇、苯、己烯三种无色液体的一种试剂是( )
| A. | 金属钠 | B. | 氢氧化钠溶液 | C. | 盐酸 | D. | 溴水 |
10.下列氢化物中,最稳定的是( )
| A. | HCl | B. | HI | C. | NH3 | D. | HF |
11.化学与环境、材料、信息、能源关系密切,下列说法正确的是( )
| A. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| B. | 蛋白质和油脂都属于高分子化合物,一定条件下都能水解 | |
| C. | PM 2.5是指大气中直径接近2.5×10-6m的颗粒物,分散在空气中形成胶体 | |
| D. | 聚乙烯食品包装袋、食物保鲜膜都是无毒的高分子化合物 |