题目内容
2.在一密闭容器中,反应m A(g)+n B(g)?3C(g)达到平衡时,测得c(A)=0.5mol/L.在温度不变的情况下,将容器体积增大一倍,当达到新的平衡时,测得c(A)=0.20mol/L.下列判断中正确的是( )| A. | A的质量分数增大 | B. | 化学计量数:m+n>3 | ||
| C. | 平衡向右移动 | D. | 物质C的体积分数减小 |
分析 保持温度不变,将容器增大一倍,当达到新的平衡时,如平衡不移动,A的浓度为0.25mol/L,大于实际A的浓度变为0.2mol/L,说明平衡向消耗A的方向移动,即向正反应移动,据此结合选项解答.
解答 解:保持温度不变,将容器增大一倍,当达到新的平衡时,如平衡不移动,A的浓度为0.25mol/L,大于实际A的浓度变为0.2mol/L,说明平衡向消耗A的方向移动,即向正反应移动
A、由上述分析可知,平衡向正反应方向移动,A的质量分数减小,故A错误;
B、增大体积,压强减小,平衡向正反应移动,压强减小平衡向气体物质的量增大的方向移动,即m+n<3,故B错误;
C、由上述分析可知,平衡向正反应方向移动即向右移动,故C正确;
D、由上述分析可知,平衡向正反应方向移动,C的体积分数增加,故D错误;
故选C.
点评 本题考查化学平衡移动,难度中等,利用假设法判断平衡移动方向是解题关键.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
16.在含c(NH4Cl)=2c(AlCl3)的溶液中滴加NaOH溶液.下列离子方程式不符合实际情况的是( )
| A. | Al3++2NH4++5OH-=Al(OH)3↓+2NH3•H2O | |
| B. | 2Al3++NH4++7OH-=2Al(OH)3+NH3•H2O | |
| C. | Al3++4NH4++8OH-=4NH3•H2O+AlO2-+2H2O | |
| D. | Al3++2NH4++6OH-=AlO2-+2NH3•H2O+2H2O |
10.0.96g Mg跟含6.3g HNO3的稀溶液恰好反应完全,则HNO3的还原产物的摩尔质量可能是( )
| A. | 30 g•mol-1或46 g•mol-1 | B. | 44 g•mol-1或80 g•mol-1 | ||
| C. | 28 g•mol-1 | D. | 46 g•mol-1 |
17.下列表示对应化学反应的离子方程式正确的是( )
| A. | 用KIO3氧化酸性溶液中的KI:5I-+IO${\;}_{3}^{+}$+3H2O═3I2+6OH- | |
| B. | 向NH4HSO3溶液中加过量的NaOH溶液并加热:NH${\;}_{4}^{+}$+OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 将过量SO2通入冷氨水中:SO2+NH3•H2O═HSO${\;}_{3}^{-}$+NH${\;}_{4}^{+}$ | |
| D. | Ba(OH)2溶液中逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的OH-恰好反应一半时:Ba2++2OH-+2H++SO${\;}_{4}^{2-}$═BaSO4↓+2H2O |
14.已知燃烧7.80乙炔气体生成二氧化碳气体和液态水时,放出389.9KJ热量,则下列有关乙炔气体燃烧的热化学方程式中,正确的是( )
| A. | 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H═-2599.2 kJ•mol-1 | |
| B. | 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H═-389.9 kJ•mol-1 | |
| C. | C2H2(g)+5/2 O2(g)═2CO2(g)+H2O(l)△H═-1299.6 kJ•mol-1 | |
| D. | 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(g)△H═-1299.6kJ•mol-1 |
11.已知热化学方程式:aX(g)+3Y(s)?bZ(g)△H<0.现在2L的密闭容器中加入0.9mol的X和1mol的Y,当Y的物质的量减少0.75mol时,达到平衡状态,此时X、Z的浓度分别是0.2mol/L和0.5mol/L,该温度下的平衡常数为( )
| A. | $\frac{25}{16}$ | B. | $\frac{5}{4}$ | C. | 35 | D. | 20 |
12.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 25℃时,1L pH=1的H2SO4溶液中,SO42-数目为0.1NA | |
| B. | 将7.8gNa2O2放入足量的CO2和水蒸气组成的气体中充分反应,转移电子总数为0.1 NA | |
| C. | 9g重氧水(H218O)含电子总数为10 NA | |
| D. | 常温常压下,2.24L正戊烷、异戊烷及新戊烷的混合物,含C-H数目为1.2 NA |
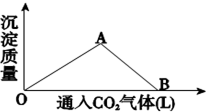 如图为一定量饱和 Ca(OH)2溶液中通入二氧化碳气体后,产生 CaCO3 白色沉淀的质量与二氧化碳体积之间的关系曲线.
如图为一定量饱和 Ca(OH)2溶液中通入二氧化碳气体后,产生 CaCO3 白色沉淀的质量与二氧化碳体积之间的关系曲线.