题目内容
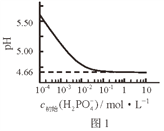
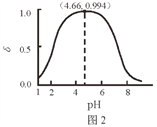
【题目】LiH2PO4是制备电池的重要原料。室温下,LiH2PO4溶液的pH随c初始(H2PO4–)的变化如图1所示,H3PO4溶液中H2PO4–的分布分数δ随pH的变化如图2所示,[![]() ]下列有关LiH2PO4溶液的叙述正确的是
]下列有关LiH2PO4溶液的叙述正确的是
A. 溶液中存在3个平衡
B. 含P元素的粒子有H2PO4–、HPO42–、PO43–
C. 随c初始(H2PO4–)增大,溶液的pH明显变小
D. 用浓度大于1 mol·L-1的H3PO4溶液溶解Li2CO3,当pH达到4.66时,H3PO4几乎全部转化为LiH2PO4
【答案】D
【解析】分析:本题考查电解质溶液的相关知识。应该从题目的两个图入手,结合磷酸的基本性质进行分析。
详解:A.溶液中存在H2PO4–的电离平衡和水解平衡,存在HPO42–的电离平衡,存在水的电离平衡,所以至少存在4个平衡。选项A错误。
B.含P元素的粒子有H2PO4–、HPO42–、PO43–和H3PO4。选B错误。
C.从图1中得到随着c初始(H2PO4–)增大,溶液的pH不过从5.5减小到4.66,谈不上明显变小,同时达到4.66的pH值以后就不变了。所以选项C错误。
D.由图2得到,pH=4.66的时候,δ=0.994,即溶液中所有含P的成分中H2PO4–占99.4%,所以此时H3PO4几乎全部转化为LiH2PO4。选项D正确。

练习册系列答案
相关题目