题目内容
【题目】在200 mL由NaCl、MgCl2、KCl组成的混合液中,部分离子浓度大小如图所示,回答下列问题:
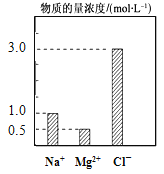
(1)该混合液中,NaCl的物质的量的浓度为 molL-1,含溶质MgCl2的物质的量为 mol。
(2)该混合液中KCl的质量为 g。
【答案】(1)1.0;0.1 (2) 14.9
【解析】
试题分析:(1)根据图像可知,Na+的物质的量浓度为1.0mol/L,则该混合液中,NaCl的物质的量的浓度为1.0molL-1,同理,MgCl2的物质的量浓度为0.5mol/L,含溶质MgCl2的物质的量为0.5mol/L×0.2L=0.1mol。(2)根据溶液呈电中性,则c(K+) + 2c(Mg2+) + c(Na+) = c(Cl-) , c(K+) = 3.0 - 1.0 - 0.5 × 2 = 1.0 mol/L,所以该混合液中KCl的质量为1.0mol/L×0.2L×74.5g/mol=14.9g。

练习册系列答案
相关题目