题目内容
9.下列化学用语正确的是( )| A. | Mg2+的电子式:Mg2+ | B. | 乙烯的结构简式:CH2CH2 | ||
| C. | 丙烷的分子式:CH3CH2CH3 | D. | CH4的立体结构式: |
分析 A.镁离子为简单阳离子,其电子式直接用离子符号表示;
B.乙烯的结构简式中没有表示出碳碳双键;
C.丙烷的分子式只表示出含有元素种类及数目即可,CH3CH2CH3为丙烷的结构简式;
D.用短线代替所有共用电子对即为结构式,据此判断甲烷的结构式;
解答 解:A.镁离子为简单阳离子,其电子式为:Mg2+,故A正确;
B.乙烯分子中含有碳碳双键,其正确的结构简式为:CH2=CH2,故B错误;
C.CH3CH2CH3为丙烷的结构简式,丙烷的分子式为:C3H8,故C错误;
D.甲烷是碳原子和氢原子间通过共价单键形成的空间正四面体结构,甲烷的结构式为: ,故D错误;
,故D错误;
故选A.
点评 本题考查了常见化学用语的表示方法判断,题目难度中等,注意掌握结构式、结构简式、电子式、分子式的书写原则,明确结构简式与结构式、分子式的区别,试题侧重考查学生规范答题的能力.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
5.关于反应中的先后顺序,下列评价正确的是( )
| A. | 向浓度都为0.1mol•L-1Na2CO3和NaOH混合溶液中通入CO2,NaOH首先反应 | |
| B. | 向NH4Al(SO4)2溶液中滴加少量的NaOH溶液,NH4+首先反应 | |
| C. | 向浓度都为0.1mol•L-1的FeCl3和CuCl2混合溶液中加入铁粉,CuCl2首先反应 | |
| D. | 向0.1mol•L-1的FeCl3溶液中加入质量相同、颗粒大小相同的铁和铜,铜首先反应 |
6.25℃时,H2SO3及其钠盐的溶液中,H2SO3、HSO3-、SO32-的物质的量分数(α)随溶液pH变化关系如图所示,下列叙述错误的是( )
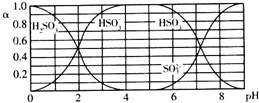

| A. | 溶液的pH=5时,硫元素的主要存在形式为HSO3- | |
| B. | 当溶液恰好呈中性时:c(Na+)>c(SO32-)+c(HSO3-) | |
| C. | 向pH=8的上述溶液中滴加少量澄清石灰水,$\frac{{c({HSO_3^-})}}{{c({SO_3^{2-}})}}$的值增大 | |
| D. | 向pH=3的上述溶液中滴加少量稀硫酸,α(HSO3-)减小 |
17.如图是某化学兴趣小组制备PCl3的实验装置(部分仪器已省略):

有关物质的部分性质如下:
请回答下列问题:
(1)仪器戊的名称为冷凝管.
(2)实验时甲中所发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(3)乙中盛放的试剂是饱和氯化钠溶液,其作用是除去氯气中的氯化氢;丙中盛放的试剂是浓硫酸,其作用是除去氯气中的水蒸气.
(4)向仪器丁中通入干燥、纯净的Cl2之前,应先通入一段时间的CO2,其目的主要是排净装置中的空气,防止空气中的水分和氧气与PCl3反应.
(5)碱石灰的作用是吸收多余的Cl2,防止污染环境;防止空气中的水蒸气进入影响产品纯度(答出一条即可).
(6)PCl3粗产品中常含有POCl3、PCl5等,加入黄磷(化学式用P表示)经加热除去PCl5的化学反应方程式为3PCl5+2P$\frac{\underline{\;\;△\;\;}}{\;}$5PCl3,后通过蒸馏(填实验操作名称),即可得到PCl3纯品.

有关物质的部分性质如下:
| 熔点/℃ | 沸点/℃ | 其他 | |
| 黄磷 | 44.1 | 280.5 | 2P(过量)+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2PCl3;2P+5Cl2(过量)$\frac{\underline{\;\;△\;\;}}{\;}$2PCl5 |
| PCl3 | -112 | 75.5 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
| POCl3 | 2 | 105.3 | 遇水生成H3PO4和HCl,能溶于PCl3 |
(1)仪器戊的名称为冷凝管.
(2)实验时甲中所发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(3)乙中盛放的试剂是饱和氯化钠溶液,其作用是除去氯气中的氯化氢;丙中盛放的试剂是浓硫酸,其作用是除去氯气中的水蒸气.
(4)向仪器丁中通入干燥、纯净的Cl2之前,应先通入一段时间的CO2,其目的主要是排净装置中的空气,防止空气中的水分和氧气与PCl3反应.
(5)碱石灰的作用是吸收多余的Cl2,防止污染环境;防止空气中的水蒸气进入影响产品纯度(答出一条即可).
(6)PCl3粗产品中常含有POCl3、PCl5等,加入黄磷(化学式用P表示)经加热除去PCl5的化学反应方程式为3PCl5+2P$\frac{\underline{\;\;△\;\;}}{\;}$5PCl3,后通过蒸馏(填实验操作名称),即可得到PCl3纯品.
4.下列图示试验正确的是( )
| A. |  制取收集干燥氨气 | B. |  碳酸氢钠受热分解 | ||
| C. |  除去CO气体中的CO2气体 | D. | 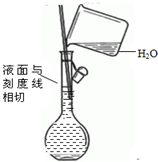 配制溶液 |
14.表示对应化学反应的离子方程式正确的是( )
| A. | FeCl2酸性溶液放在空气中变质:2Fe2++4H++O2═2Fe3++2H2O | |
| B. | 用酸性K2Cr2O7溶液检验酒精:3CH3CH2OH+2Cr2O72-+13H+═4Cr3++11H2O+3CH3COO- | |
| C. | 用惰性电极电解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+ | |
| D. | 钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-═Fe3+ |
1.下列烃中,一卤代物的同分异构体的数目最少和最多的分别是( )
| A. | 乙烷 | B. | 2-甲基丙烷 | C. | 2,2-二甲基丙烷 | D. | 2,2-二甲基丁烷 |
18.美国科学家将铅和氪两种元素的原子核对撞,获得了一种质子数为118、质量数为293的新元素,该元素原子核内的中子数为( )
| A. | 47 | B. | 57 | C. | 61 | D. | 175 |
19.某强酸性溶液X中含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行连续实验,实验内容如下:

根据以上信息,下列观点正确的是( )

根据以上信息,下列观点正确的是( )
| A. | 沉淀G的化学式为Fe(OH)2 | |
| B. | 生成气体A的离子方程式为2Fe2++NO3-+4H+=2Fe3++NO↑+2H2O | |
| C. | 反应②中的离子方程式有AlO2-+CO2+2H2O=Al(OH)3+HCO3- | |
| D. | 溶液X中,除H+ 外还肯定含有的离子是NH4+、Fe2+、SO42-. |