题目内容
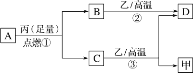
【题目】己知图甲表示某温度下pH=l的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,图乙表示水在不同温度下的电离平衡曲线。下列有关图像的判断叙述正确的是
A.图甲中曲线II为盐酸
B.图甲中a点溶液的导电性比b点弱
C.图乙中纯水仅升高温度,就可以从a点变到c点
D.图乙中在b点对应温度下,将pH=2的H2SO4溶液与pH=10的NaOH溶液等体积混合后,溶液显中性
【答案】D
【解析】
A.相同pH的盐酸和醋酸溶液分别加水稀释相同倍数时,盐酸的pH变化大,醋酸为弱酸稀释促进电离,加水稀释后醋酸pH较小,曲线II为醋酸,故A错误;
B.溶液导电性与溶液中离子浓度成正比,b点pH大于a点,b点c(H+)小于a点,b点溶液的导电性比a点弱,故B错误;
C.纯水仅升高温度,促进水解,氢离子和氢氧根离子浓度均增大,图乙中从a点变到c点氢氧根离子浓度不变,故C错误;
D.图乙中在b点对应的温度下,Kw=10-12,中性溶液pH=6;将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,c(H+)=10-2mol/L,c(OH-)=10-2mol/L浓度相同,等体积混合溶液呈中性,所以D选项是正确的。
答案选D。

【题目】CO2的回收与利用是科学家研究的热点课题,可利用CH4与CO2制备“合成气”(CO、H2),还可制备甲醇、二甲醚、低碳烯烃等燃料产品。
I.制合成气
科学家提出制备“合成气”反应历程分两步:
反应①:CH4(g)![]() C(ads)+2H2 (g) (慢反应)
C(ads)+2H2 (g) (慢反应)
反应②:C(ads)+ CO2(g)![]() 2CO(g) (快反应)
2CO(g) (快反应)
上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:
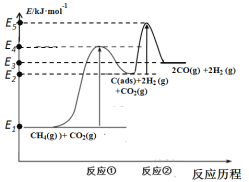
(1)CH4与CO2制备“合成气”的热化学方程式为_________。能量变化图中:E5+E1_________E4+E2(填“>”、“<”或“=”)。
II.脱水制醚
利用“合成气”合成甲醇后,甲醇脱水制得二甲醚的反应为:
2CH3OH(g)![]() CH3OCH3(g) + H2O(g) ΔH,其速率方程式为:v正= k正·c2(CH3OH),v逆=k逆·c(CH3OCH3)·c(H2O),k正、k逆为速率常数且只与温度有关。经查阅资料,上述反应平衡状态下存在计算式:lnKc = 2.205+
CH3OCH3(g) + H2O(g) ΔH,其速率方程式为:v正= k正·c2(CH3OH),v逆=k逆·c(CH3OCH3)·c(H2O),k正、k逆为速率常数且只与温度有关。经查阅资料,上述反应平衡状态下存在计算式:lnKc = 2.205+![]() (Kc为化学平衡常数;T 为热力学温度,单位为K)。
(Kc为化学平衡常数;T 为热力学温度,单位为K)。
(2)反应达到平衡后,仅升高温度,k正增大的倍数_________ k逆增大的倍数(填“>”、“<”或“=”)。
(3)某温度下(该反应平衡常数Kc为200),在密闭容器中加入一定量 CH3OH,反应到某时刻测得各组分的物质的量如下:
物质 | CH3OH | CH3OCH3 | H2O |
物质的量/mol | 0.4 | 0.4 | 0.4 |
此时正、逆反应速率的大小:v正 ____v逆 (填“>”、 “<”或“=”)。
(4)500K下,在密闭容器中加入一定量甲醇 CH3OH,反应到达平衡状态时,体系中CH3OCH3(g)的物质的量分数为_________(填标号)。
A <![]() B
B ![]() C >
C >![]() D 无法确定
D 无法确定