题目内容
【题目】已知如下反应,回答下列问题:
3I2 + 6NaOH = 5NaI + NaIO3 + 3H2O
(1)画出这个反应的双线桥___________
(2)_______是氧化剂,氧化产物是___________;
(3)氧化剂与还原剂的物质的量之比为____________,当反应消耗3mol NaOH时,转移的电子数目为_________________
【答案】 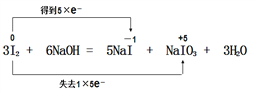 I2 NaIO3 5:1 2.5NA
I2 NaIO3 5:1 2.5NA
【解析】(1)用双线桥表示这个反应的电子转移的方向和数目为: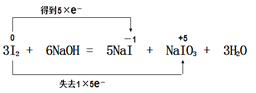
(2)该反应中碘的化合价部分升高、部分降低,所以I2既是氧化剂又是还原剂,氧化产物是NaIO3 、还原产物为NaI;
(3)根据还原产物和氧化产物的物质的量之比为5:1,可知氧化剂与还原剂的物质的量之比为5:1。该反应中电子转移的数目为5e-,所以当反应消耗3mol NaOH时,转移的电子数目为2.5NA.

练习册系列答案
相关题目
