��Ŀ����
����Ŀ��CuCl�㷺Ӧ���ڻ�����ӡȾ����ҵ��ij�о�С���ô�ͭ(������Fe) Ϊԭ���Ʊ�CuCl2��2H2O���壬����CuCl2��2H2O�����Ʊ�CuCl��
(1)�Ʊ�CuCl2��2H2O���壺
�� Bװ���з�����Ӧ�Ļ�ѧ����ʽ��_________________
�� װ��C�д�ͭ��ĩ(������Fe)�������ַ�Ӧʱ����������______________
�� ��Ӧ��ɺ�C�еĹ�����ϡ������ȫ�ܽ⣬�ٵ���pHֵ���ӣ���һϵ�в�����ɻ��CuCl2��2H2O���塣�ܽ�C�����������ʱ����ʱ���������˫��ˮ��Ŀ����__________
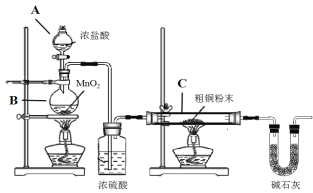
(2)��ȡCuCl��Ϊ����ȡCuCl������ͼ��ʾװ�ý���ʵ��(�г�������)��
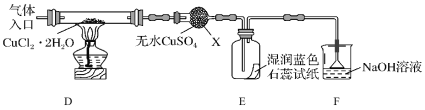
��֪��![]()
������X��������__________
��ʵ��������Ⱥ�˳����a��__________________________��e(������ı��)��
a�����װ�õ������Ժ����ҩƷ b��Ϩ��ƾ��ƣ���ȴ
c�����������������ͨ�����HCl d����ȼ�ƾ��ƣ�����
e��ֹͣͨ��HCl��Ȼ��ͨ��N2
��װ��F��NaOH��Һ��������___________________��
�� ��Ӧ������ȡ��CuCl��Ʒ����ʵ�飬�������к���������CuCl2��CuO���ʡ����������CuCl2���ʵ�ԭ����__________________________
���𰸡�MnO2+4HCl(Ũ) ![]() MnCl2+Cl2��+2H2O FeCl3 ��CuCl2 ����Ԫ��ת��ΪFe3+ ���θ���� c��d��b ����HCl��Cl2 ����ʱ�䲻����¶�ƫ��
MnCl2+Cl2��+2H2O FeCl3 ��CuCl2 ����Ԫ��ת��ΪFe3+ ���θ���� c��d��b ����HCl��Cl2 ����ʱ�䲻����¶�ƫ��
��������
(1)Bװ�����Ʊ�������װ�ã�Ũ�����ܹ���ȥ�����е�ˮ�����������������C����ͭ������Ӧ�����Ȼ������Ȼ�ͭ����ʯ�ҿ��Է�ֹ�����е�ˮ��������װ��C�У�ͬʱ���Գ�ȥδ��Ӧ����������ֹ��Ⱦ���ݴ˷������١��ۣ�
(2)�������⣬�ȷֽ�CuCl22H2O�Ʊ�CuCl����Ҫ����Cu2+ˮ�⣬���������Ҫͨ��HCl���壬Ȼ�����A���Թܣ�X����ˮ����ͭ���������Լ���CuCl22H2O�ֽ����ɵ�ˮ������E����ֽ�ȱ�����ɫ��˵��CuCl2�ֽ�������Cl2��F��NaOH��Һ��������β������ֹ��Ⱦ���ݴ˷������ܡ��ߡ�
(1)��Բ����ƿ��Ũ����Ͷ������̻�ϼ��ȷ�Ӧ�����������Ȼ��̣���Ӧ�Ļ�ѧ��ʽΪ4HCl+MnO2 ![]() MnCl2+Cl2��+2H2O���ʴ�Ϊ��4HCl+MnO2
MnCl2+Cl2��+2H2O���ʴ�Ϊ��4HCl+MnO2 ![]() MnCl2+Cl2��+2H2O��
MnCl2+Cl2��+2H2O��
�ڴ�ͭ�е�Cu��Fe�����ڼ�����������������Ӧ����Ӧ����Ϊ�Ȼ�ͭ���Ȼ������ʴ�Ϊ��CuCl2��FeCl3��
�۷�Ӧ��ɺ�C�еĹ���(����δ��Ӧ����)��ϡ������ȫ�ܽ⣬��Һ�к���CuCl2��FeCl3��FeCl2������pHֵ���ӣ���Ҫ���Ƚ�������������ת��Ϊ�����ӣ���˼�������˫��ˮ��������Һ�п��ܺ��е�Fe2+������ͨ��������ҺpH��ȥ���ʴ�Ϊ��������Һ�п��ܺ��е�Fe2+��
(2)����ͼ��������������֪������X������Ϊ���θ���ܣ��ʴ�Ϊ�����θ���ܣ�
��ʵ�������������ɣ���Ҫ�ȼ��װ�õ������ԣ����ȷֽ�CuCl22H2O�Ʊ�CuCl����Ҫ��ֹCu2+ˮ���CuCl�����������Ա���Ҫ�ȸ���װ���е�������ˮ��������ܼ��ȣ�������HCl�����м����Ʊ�����Ӧ��������Ϩ��ƾ��ƣ�����ͨ�뵪��ֱ��װ����ȴ�����Բ���˳��Ϊ��a��c��d��b��e���ʴ�Ϊ��c��d��b��
���ȷֽ�CuCl22H2O�Ʊ�CuCl�����л�����������Ȼ������Ⱦ���������壬װ��F��NaOH��Һ��������HCl��Cl2����ֹ��Ⱦ���ʴ�Ϊ������HCl��Cl2��
����2CuCl2 ![]() 2CuCl+Cl2������������CuCl2��˵��CuCl2û�з�Ӧ��ȫ���ֽⲻ��֣��ʴ�Ϊ������ʱ�䲻����¶�ƫ�͡�
2CuCl+Cl2������������CuCl2��˵��CuCl2û�з�Ӧ��ȫ���ֽⲻ��֣��ʴ�Ϊ������ʱ�䲻����¶�ƫ�͡�

 �������ͬ������ϵ�д�
�������ͬ������ϵ�д�����Ŀ���̲��ں��Ĵ�������ȼ�������俪�������ǵ�ǰ�����ԴΣ������Ҫ���⡣CH4(g)+2H2O(g)![]() CO2(g)+4H2(g) ��H3 = +a kJ��mol-1
CO2(g)+4H2(g) ��H3 = +a kJ��mol-1
��ѧ�� | C��H | H��H | H��O |
����kJ/mol | b | c | d |
(1)д������Ľṹʽ___________
(2)C=O�ļ���Ϊ_______________kJ/mol (�ú�a��b��c��d��ʽ�ӱ�ʾ)
(3)���������£��������Ϊ0.5L���ܱ�������ͨ��һ���������ˮ����������������Ӧ����ü������ʵ�����ʱ��仯���±���ʾ��0��10min����H2O��Ũ�ȱ�ʾ�÷�Ӧ��ƽ������Ϊ��(H2O)= _____________
ʱ��/min | 0 | 10 | 20 | 40 | 50 | 60 |
n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 | 0.10 |
(4)���º�������£�����������˵���˷�Ӧ�ﵽƽ��״̬����_______________��
a����������ƽ����Է����������ֲ��� b��CO2��H2�����������Ϊ1�s4
c�����������ܶȱ��ֲ��� d��1mol CO2���ɵ�ͬʱ��4mol H-H������
����Ŀ������ʵ���������ý��۾���ȷ���ǣ� ��
ʵ�� | ʵ������ | ���� |
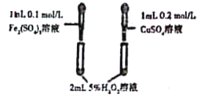
A�� | ����Թܱ��Ҳ��Թ��в������ݵ����ʿ� | Fe3+��H2O2�ֽ�Ĵ�Ч������ |
B�� | �������Ϊ��ɫ���Ҳ�����Ϊ��ɫ | �����ԣ�Cl2>Br2> I2 |
C�� | U�ι����Һ���½�,�Ҷ�Һ������ | NH4NO3�ܽ����� |
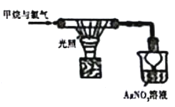
D�� | �ձ��в�����ɫ���� | �������������������·���ȡ����Ӧ |
A.AB.BC.CD.D