题目内容
10.下列变化是通过取代反应来实现的是( )| A. | 在镍做催化剂的条件下,苯与氢气反应 | |
| B. | 苯与液溴混合后加入铁粉 | |
| C. | 乙烯通入溴水中 | |
| D. | 烧至红热的铜丝插入乙醇中 |
分析 有机物中的原子或原子团被其他的原子或原子团所代替生成新的化合物的反应叫取代反应,结合各物质的性质分析.
解答 解:A、在镍做催化剂的条件下,苯与氢气反应生成环己烷,属于加成反应,故A错误;
B、苯与液溴反应,苯环上的氢原子被溴原子取代取代生成溴苯,属于取代反应,故B正确;
C、乙烯与溴水发生加成反应生成1,2-二溴乙烷,故C错误;
D、乙醇在催化剂作用下与氧气反应生成乙醛,该反应为氧化反应,故D错误;
故选B
点评 本题考查了取代反应的判断,题目难度不大,注意掌握常见的有机物的性质,明确取代反应和加成反应的区别.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
20.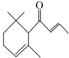 一种从植物中提取的天然化合物αdamascone可用于制作“香水”,其结构简式如图.有关该化合物的下列说法不正确的是( )
一种从植物中提取的天然化合物αdamascone可用于制作“香水”,其结构简式如图.有关该化合物的下列说法不正确的是( )
 一种从植物中提取的天然化合物αdamascone可用于制作“香水”,其结构简式如图.有关该化合物的下列说法不正确的是( )
一种从植物中提取的天然化合物αdamascone可用于制作“香水”,其结构简式如图.有关该化合物的下列说法不正确的是( )| A. | 分子式为C13H20O | |
| B. | 该化合物可发生加聚反应 | |
| C. | 1 mol该化合物完全燃烧消耗18molO2 | |
| D. | 该物质能使溴水和酸性KMnO4溶液褪色 |
15.常温下,下列有关叙述正确的是( )
| A. | pH相等的①NH4NO3、②(NH4)2SO4、③NH4HSO4三溶液中,c(NH4+)大小顺序为:①>②>③ | |
| B. | Na2CO3溶液中,2c(Na+)═c(CO32-)+c(HCO3-)+c(H2CO3) | |
| C. | NaB溶液的pH=8,c(Na+)-c(B-)=9.9×10-7 mol/L | |
| D. | 10 mL pH=12NaOH溶液中加入pH=2的HA溶液至pH刚好等于7,则溶液体积V(总)=20 mL |
20.饮水安全在人们生活中占有极为重要的地位,某研究小组提取三处被污染的水源进行了分析,给出了如下实验信息:其中一处被污染的水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质.A、B、C、D、E五种常见化合物都是由下表中的离子形成:(其中一种物质为复盐)
为了鉴别上述化合物,分别进行以下实验,其结果如下所示:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃片);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成.根据上述实验填空:
(1)写出B、D的化学式:B:KNO3、D:CuSO4.
(2)将含1mol A的溶液与含1mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为Na2CO3 .
(3)写出实验②发生反应的离子方程式Al3++3OH-═Al(OH)3↓,Al(OH)3+OH-═[Al(OH)4]-.
(4)向D的溶液中加入过量氨水反应的离子方程式为Cu2++2NH3•H2O═Cu(OH)2↓+2NH4+、Cu(OH)2+4NH3.H2O?[Cu(NH3)4]2++2OH-+4H2O.
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 | SO42- HCO3- NO3- OH- |
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃片);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成.根据上述实验填空:
(1)写出B、D的化学式:B:KNO3、D:CuSO4.
(2)将含1mol A的溶液与含1mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为Na2CO3 .
(3)写出实验②发生反应的离子方程式Al3++3OH-═Al(OH)3↓,Al(OH)3+OH-═[Al(OH)4]-.
(4)向D的溶液中加入过量氨水反应的离子方程式为Cu2++2NH3•H2O═Cu(OH)2↓+2NH4+、Cu(OH)2+4NH3.H2O?[Cu(NH3)4]2++2OH-+4H2O.
 .
. .
. .
.