题目内容
8.能用浓硫酸干燥的一组气体是( )| A. | H2和NH3 | B. | H2,SO2和CO | C. | H2S和SO2 | D. | NH3,H2S和SO2 |
分析 浓硫酸具有酸的通性、吸水性.脱水性和强氧化性,所以浓硫酸不能干燥具有碱性、还原性的气体.
解答 解:A.氨气为碱性气体,不能用浓硫酸干燥,故A错误;
B.H2和CO为中性气体,SO2为酸性氧化物,可用浓硫酸干燥,故B正确;
C.硫化氢为酸性且有还原性的气体,能被浓硫酸氧化,不能用浓硫酸干燥,故C错误;
D.氨气为碱性气体,不能用浓硫酸干燥硫化氢为酸性且有还原性的气体,能被浓硫酸氧化,不能用浓硫酸干燥,故D错误.
故选B.
点评 本题考查气体除杂问题,水蒸汽的吸收比较复杂,中性气体可用浓硫酸、五氧化二磷、无水氯化钙或碱石灰干燥;酸性气体可用浓硫酸或五氧化二磷或无水氯化钙干燥,碱性气体NH3碱石灰干燥;能被浓硫酸氧化,能被碱石灰吸收的还原性气体一般用五氧化二磷或无水氯化钙干燥,题目难度不大.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
18.已知,常温下,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.3×10-17,下列叙述中正确的是( )
| A. | 常温下,AgCl在饱和NaCl溶液中的Ksp比在纯水中的Ksp小 | |
| B. | 向AgCl的悬浊液中加入KI溶液,沉淀由白色转化为黄色 | |
| C. | 将0.001 mol•L-1的AgNO3溶液滴入KCl和KI的混合溶液中,一定先产生AgI沉淀 | |
| D. | 向AgCl的饱和溶液中加入NaCl晶体,有AgCl析出且溶液中c(Ag+)=c(Cl-) |
16.家里的食用花生油中如果混有水份,可以采用下列何种方法分离( )
| A. | 过滤 | B. | 蒸馏 | C. | 分液 | D. | 结晶 |
3.已知链式炔碳C300经过适当处理可得含多个-C≡C-(不含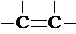 )的链状化合物C300H298,则含-C≡C-的个数为( )
)的链状化合物C300H298,则含-C≡C-的个数为( )
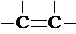 )的链状化合物C300H298,则含-C≡C-的个数为( )
)的链状化合物C300H298,则含-C≡C-的个数为( )| A. | 70 | B. | 72 | C. | 74 | D. | 76 |
13.为检验Na2SO3溶液中是否混有Na2SO4,应使用的试剂是( )
| A. | BaCl2溶液 | B. | Ba(NO3)2溶液 | ||
| C. | BaCl2溶液和稀H2SO4 | D. | BaCl2溶液和稀盐酸 |
18.一种用于制造隐形飞机的材料其主要成分的分子结构如图,它属于( )


| A. | 无机物 | B. | 烯烃 | C. | 高分子化合物 | D. | 有机化合物 |