题目内容
【题目】在密闭容器发生下列反应:aA(g)![]() cC(g)+dD(g),反应达到平衡后,将容器体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将容器体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
A. 平衡向正反应方向移动
B. a<c+d
C. D的体积分数增大
D. A的转化率变大
【答案】B
【解析】试题分析:假定平衡不移动,将气体体积压缩到原来的一半,D的浓度为原来的2倍,实际再次达到新平衡时,D的浓度为原来的1.8倍,说明压强增大,平衡向逆反应移动,即a<c+d,压强增大,速率加快,新平衡的正、逆速率都大于原平衡;A.气体体积压缩到原来的一半,D的浓度为原来的1.8倍,说明压强增大,平衡向逆反应移动,故A错误;B.气体体积压缩到原来的一半,D的浓度为原来的1.8倍,说明压强增大,平衡向逆反应移动,反应物气体体积小于生成物,a<c+d,故B正确;C.气体体积压缩到原来的一半,D的浓度为原来的1.8倍,说明压强增大,平衡向逆反应移动,D体积分数减小,故C错误;D.平衡向逆反应移动,A的转化率降低,故D错误;故选B。

【题目】工业上可用焦炭、二氧化硅的混合物在高温下与氧气反应生成SiCl4,SiCl4经提纯后用氢气还原得高纯硅。以下是某化学小组制备干景的氧气并在实验室制备SiCl4的部分装置示意图(注: SiCl4遇水易水解)。

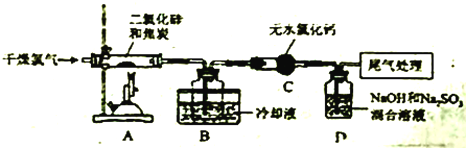
(1)选择上图部分装置,制备纯净干燥的氯气,正确的仪器连接顺序为:发生装置甲→___→____→_____→_____→装置A(用小写字母填空)。_____________
(2)上图C装置的作用是_______________。
(3)装置A的硬质玻璃管中二氧化硅和焦炭与氯气恰好完全反应生成SCl4,则二氧化硅和碳的物质的量之比为_________________。
(4)经过讨论,该小组认为D中吸收尾气一段时间后,除了过量的OH-,吸收液中阴离子肯定存在Cl-和SO42-,原因是__________(用离子方程式解释)。
(5)有同学认为可能还存在其它酸根离子(忽略空气中CO2的影响),提出下列假设(不考虑各因素的叠加),假设1:只有SO32-,假设2:只有ClO-,假设3:……
设计实验验证上述假设1和假设2:取少量吸收液于试管中,滴加3mol/LH2SO4至溶液呈酸性,然后将所得溶液分置于a、b两试管中,请填写空白的实验步骤、预期现象。
实验步骤(简述操作过程) | 预期現象 | 结论 |
向a试管中滴加几滴品红溶液,观察现象,加热试管a,观察到 | ____________。 ____________。 | 假设1成立 |
向b试管中滴加______________ | 溶液变为蓝色。 | 假设2成立 |