题目内容
高铁酸钠(Na2FeO4)是一种高效的饮用水处理剂,工业上可由下列方法制得:Fe2O3+3Na2O2 2Na2FeO4+Na2O
2Na2FeO4+Na2O
关于该反应说法正确的是
| A.反应中Na2O2是氧化剂 |
| B.Fe2O3可以通过铁丝在氧气中燃烧制得 |
| C.生成1 mol Na2FeO4,有6 mol电子转移 |
| D.在Na2FeO4中Fe为+4价,具有强氧化性,能消毒杀菌 |
A
解析试题分析:A在该反应中Na2O2作氧化剂,把Fe2O3氧化为Na2FeO4,它本身被还原为Na2O。正确。B、Fe2O3可以通过铁丝在氧气中加热制得。燃烧则产生四氧化三铁。错误。C反应前铁的化合价为+3价,反应后变为Na2FeO4中的+6价。故生成1 mol Na2FeO4,有3mol电子转移.错误。D、在Na2FeO4中Fe为+6价,具有强氧化性,能消毒杀菌,还原产物氢氧化铁有吸附性,又可以起到净化水的作用。错误。
考点:考查高效的饮用水处理剂高铁酸钠(Na2FeO4)的制备及性质的知识。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案
相关题目
在空气中,有下列反应发生:①N2+O2=2NO;②2NO+O2=2NO2;③3NO2+H2O=2HNO3+NO;④2SO2+O2=2SO3;⑤SO3+H2O=H2SO4;⑥SO2+H2O=H2SO3;⑦3O2=2O3。其中属于氧化还原反应的是( )
| A.①②③④ | B.①②③④⑦ | C.①②④⑦ | D.①②③④⑤⑥⑦ |
下列氧化还原反应中,水作为氧化剂的是( )
A.CO+H2O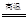 CO2+H2 CO2+H2 | B.Cl2+H2O=HCl+HClO |
| C.2Na2O2+2H2O=4NaOH+O2↑ | D.2F2+2H2O=4HF+O2 |
向Na2SO3和NaI的物质的量之比为1:1的混合溶液中逐滴滴入氯水,
下列离子反应不可能发生的是
| A.SO32- +Cl2+ H2O → SO42- +2H ++ 2Cl- |
| B.4I-+ SO32- +3Cl2+ H2O → SO42- +2H ++ 6Cl-+2I2 |
| C.2I-+ SO32- +2Cl2+ H2O → SO42- +2H ++ 4Cl-+2I2 |
| D.2I-+ 2SO32- +3Cl2+ 2H2O →2SO42- +4H ++ 6Cl-+I2 |
对剧毒的氰化物可在碱性条件下用如下方法进行处理:
2CN- +8OH-+5Cl2= 2CO2 +N2 +10Cl- +4H2O 下列判断正确的是
| A.当有0.2 mol CO2生成时,溶液中阴离子的物质的量增加1mol |
| B.该反应中,每有2molCN-反应,转移电子为10mol |
| C.上述反应中的还原剂是OH- |
| D.还原性:Cl-> CN- |
下列说法正确的是
| A.氧化还原反应的本质是有化合价的变化 |
| B.分解反应一定是氧化还原反应 |
| C.利用化合反应可制备FeCl2、Fe(OH)3 |
| D.在一定条件下能向正反两个方向进行的反应称为可逆反应 |
常温下,下列三个反应都能进行:2NaW+X2=2NaX+W2,2NaY+W2=2NaW+Y2,2KX+Z2=2KZ+X2,由此得出正确的结论是
| A.X-、Y-、Z-、W- 中Z- 的还原性最强 | B.2Z-+Y2 = 2Y-+Z2能进行 |
| C.X2、Y2、Z2、W2中Z2的氧化性最强 | D.还原性X-﹥Y- |
下列反应中必须加入还原剂才能进行的是
| A.Zn→Zn2+ | B.H2→H2O | C.CaO→Ca(OH)2 | D.CuO→Cu |