题目内容
将2.0molPCl3,和1.0molCl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)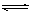 PCl5(g)达到平衡时,PCl5为0.40mol,如果此时移走1.0molPCl3和0.50molCl2,在相同温度下再达平衡时PCl5的物质的量是
PCl5(g)达到平衡时,PCl5为0.40mol,如果此时移走1.0molPCl3和0.50molCl2,在相同温度下再达平衡时PCl5的物质的量是
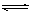 PCl5(g)达到平衡时,PCl5为0.40mol,如果此时移走1.0molPCl3和0.50molCl2,在相同温度下再达平衡时PCl5的物质的量是
PCl5(g)达到平衡时,PCl5为0.40mol,如果此时移走1.0molPCl3和0.50molCl2,在相同温度下再达平衡时PCl5的物质的量是| A.0.40mol | B.小于0.20mol | C.0.20mol | D.大于0.20mol,小于0.40mol |
B
试题分析:如果平衡时移走1.0molPCl3和0.50molCl2,就相当于开始只加入了1.0molPCl3,和0.50molCl2。与开始加入2.0molPCl3,和1.0molCl2达到平衡时,PCl5为0.40mol比较,也就是减少了反应物的浓度。假如平衡不移动,加入了1.0molPCl3,和0.50molCl2反应物的物质的量减半,生成物的物质的量也要是减半。。达到平衡时,PCl5为0.20mol,但根据平衡移动原理:增大反应物的浓度,化学平衡向正反应方向移动,减小反应物的浓度,平衡会想逆反应方向移动。所以平衡时移走1.0molPCl3和0.50molCl2在相同温度下再达平衡时PCl5的物质的量应该比0.20mol要小。选项为B。

练习册系列答案
相关题目
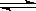 I3-(aq),某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是
I3-(aq),某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是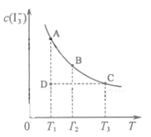
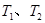 ,反应的平衡常数分别为K1、K2,则K1>K2
,反应的平衡常数分别为K1、K2,则K1>K2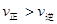
 R(g)+2L:反应符合如图所示的图象.下列叙述正确的是
R(g)+2L:反应符合如图所示的图象.下列叙述正确的是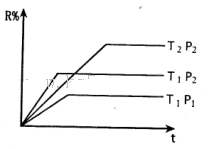
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则: I2(g)+H2(g),下列叙述能够说明已达到平衡状态的是
I2(g)+H2(g),下列叙述能够说明已达到平衡状态的是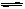 2C(g);△H=" -a" kJ/mol(a >0),在一个有催化剂的固定容积的容器中加入2mol A2和1mol B2,在500℃时充分反应达平衡后C的浓度为w mol/L,放出热量b kJ。请回答下列问题:
2C(g);△H=" -a" kJ/mol(a >0),在一个有催化剂的固定容积的容器中加入2mol A2和1mol B2,在500℃时充分反应达平衡后C的浓度为w mol/L,放出热量b kJ。请回答下列问题: