题目内容
【题目】将等物质的量的A、B 混合于 2L 的密闭容器中,发生下列反应:3A(g)+B(g) xC(g) +2D(g),经2min 后测得D 的浓度为 0.5mol·L-1,c(A)∶c(B)=3∶5,以 C 表示的平均速率 v(C)=0.25mol·L-1·min-1,下列说法正确的是( )
A.该反应方程式中,x=2B.2 min 时,A 的转化率为 50%
C.2 min 时,A 的物质的量为 0.75molD.反应速率 v(B)=0.25 mol·L-1·min-1
【答案】AB
【解析】
经2min后测得D的浓度为0.5mol/L,v(D)= ![]() =0.25molL-1min-1,C表示的平均速率v(C)=0.25molL-1min-1,由速率之比等于化学计量数之比可知,x=2,设A、B的起始物质的量均为n,生成D为2L×0.5mol/L=1mol,结合三段式分析解答。
=0.25molL-1min-1,C表示的平均速率v(C)=0.25molL-1min-1,由速率之比等于化学计量数之比可知,x=2,设A、B的起始物质的量均为n,生成D为2L×0.5mol/L=1mol,结合三段式分析解答。
经2min后测得D的浓度为0.5mol/L,v(D)=![]() =0.25molL-1min-1,C表示的平均速率v(C)=0.25molL-1min-1,由速率之比等于化学计量数之比可知,x=2,设A、B的起始物质的量均为n mol,生成D为2L×0.5mol/L=1mol,则
=0.25molL-1min-1,C表示的平均速率v(C)=0.25molL-1min-1,由速率之比等于化学计量数之比可知,x=2,设A、B的起始物质的量均为n mol,生成D为2L×0.5mol/L=1mol,则
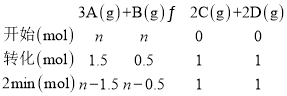
c(A)∶c(B)=3∶5,则![]() =
=![]() ,解得n=3。
,解得n=3。
A.由上述分析可知,x=2,故A正确;
B.2min时,A的转化率为![]() ×100%=50%,故B正确;
×100%=50%,故B正确;
C.2min时,A的物质的量为3mol-1.5mol=1.5mol,故C错误;
D.v(B)= =0.125molL-1min-1,故D错误;
=0.125molL-1min-1,故D错误;
故选AB。

【题目】[2016·新课标I]锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]_______________,有__________个未成对电子。
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是______________________________。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因______________________________。
GeCl4 | GeBr4 | GeI4 | |
熔点/℃ | 49.5 | 26 | 146 |
沸点/℃ | 83.1 | 186 | 约400 |
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是______________________________。
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______________,微粒之间存在的作用力是_______________。
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(![]() ,0,
,0,![]() );C为(
);C为(![]() ,
,![]() ,0)。则D原子的坐标参数为_______________。
,0)。则D原子的坐标参数为_______________。

②晶胞参数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a=565.76 pm,其密度为_____g·cm3(列出计算式即可)。