题目内容
 1L某混合溶液,可能含有的离子如下表:
1L某混合溶液,可能含有的离子如下表:| 可能大量含有的阳离子 | H+、K+、Mg2+、Al3+、NH4+、Fe2+、Fe3+ |
| 可能大量含有的阴离子 | Cl-、Br-、I-、CO32-、AlO2- |
考点:物质的检验和鉴别的实验方案设计
专题:物质检验鉴别题
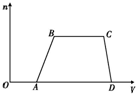
分析:开始加入NaOH没有沉淀和气体产生,则一定有H+,则无CO32-、AlO2-,后来有沉淀产生且最后消失,则一定没有Mg2+、Fe2+、Fe3+,有Al3+;B→C沉淀的质量不变,应为NH4++OH-=NH3?H2O的反应,则有NH4+,以此来解答.
解答:
解:根据图象,开始加入NaOH没有沉淀和气体产生,则一定有H+;后来有沉淀产生且最后消失,则一定没有Mg2+、Fe2+、Fe3+,有Al3+;B→C沉淀的质量不变,应为NH4++OH-=NH3?H2O的反应,则有NH4+;现象无法知道有无K+,因为有H+,则无CO32-、AlO2-,
综上所述,则该溶液中确定含有的离子是H+、Al3+、NH4+; 一定不含有的阳离子是Mg2+、Fe2+、Fe3+;一定不存在的阴离子是CO32-、AlO2-,
故答案为:H+、Al3+、NH4+; Mg2+、Fe2+、Fe3+;CO32-、AlO2-; NH4++OH-=NH3?H2O.
综上所述,则该溶液中确定含有的离子是H+、Al3+、NH4+; 一定不含有的阳离子是Mg2+、Fe2+、Fe3+;一定不存在的阴离子是CO32-、AlO2-,
故答案为:H+、Al3+、NH4+; Mg2+、Fe2+、Fe3+;CO32-、AlO2-; NH4++OH-=NH3?H2O.
点评:本题考查离子检验试验方案的设计,为高频考点,把握实验中发生的反应及离子的检验方法为解答的关键,侧重分析与实验能力的考查,注意图象与反应的对应关系及反应的先后顺序,题目难度不大.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
下列有关铝及其化合物的叙述正确的是( )
| A、铝粉与氧化镁共热可制取金属镁 |
| B、足量铝分别与含1mol HCl、1mol NaOH的溶液反应,产生相同量的氢气 |
| C、在浓硝酸中加入等体积的浓硫酸后,立即加入铝片,铝片表面发生钝化 |
| D、工业上用电解熔融Al2O3的方法冶炼铝 |
氮化铝(AlN)广泛应用于电子、陶瓷等工业领域.在一定条件下,AlN可通过反应 Al2O3+N2+C→AlN+CO (未配平)合成.下列叙述正确的是( )
| A、上述反应中,1mol N2被氧化时,可以得到6mol电子 |
| B、上述反应中,被氧化与被还原的物质 物质的量之比为2:3 |
| C、每生成1mol AlN时.消耗N2的质量为14g |
| D、AlN的摩尔质量为41g |