题目内容
铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物.“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物.该药品不溶于水但能溶于人体中的胃酸.某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:
药片
淡绿色溶液
淡红色溶液
血红色溶液
溶液褪色
(1)试剂1是 ,加入新制氯水后溶液中发生的离子反应方程式是: , ;
(2)加入KSCN溶液后,在未加新制氯水的情况下,溶液中也产生了淡红色,其可能的原因是 .
药片
| 碾碎后加入试剂1 |
| 隔绝空气静置过滤 |
| KSCN |
| 新制 |
| 氨水 |
| 一段 |
| 时间后 |
(1)试剂1是
(2)加入KSCN溶液后,在未加新制氯水的情况下,溶液中也产生了淡红色,其可能的原因是
考点:二价Fe离子和三价Fe离子的检验
专题:实验题
分析:(1)根据图示分析可知,加入试剂1用于溶解药品,应该选用加入非氧化性的酸;
氯气氧化亚铁离子生成铁离子,铁离子与硫氰根离子结合生成硫氰化铁;
(2)亚铁离子具有较强的还原性,部分亚铁离子能够被空气中氧气氧化成铁离子.
氯气氧化亚铁离子生成铁离子,铁离子与硫氰根离子结合生成硫氰化铁;
(2)亚铁离子具有较强的还原性,部分亚铁离子能够被空气中氧气氧化成铁离子.
解答:
解:(1)试剂1用于溶解样品,可以选用稀盐酸或者稀硫酸;
氯气氧化亚铁离子生成铁离子,离子方程式为:2Fe2++Cl2=2Fe3++2Cl-;
铁离子与硫氰根离子结合生成硫氰化铁,离子方程式为:Fe3++SCN-=[Fe(SCN)]2+ (或Fe3++3SCN-=Fe(SCN)3),
故答案为:稀盐酸(或稀硫酸溶液);2Fe2++Cl2=2Fe3++2Cl-;Fe3++SCN-=[Fe(SCN)]2+ (或Fe3++3SCN-=Fe(SCN)3);
(2)少量亚铁离子被空气中的氧气氧化成铁离子,所以加入KSCN溶液后,在未加新制氯水的情况下,溶液中也产生了红色,
故答案为:少量Fe2+被空气中氧气氧化成Fe3+.
氯气氧化亚铁离子生成铁离子,离子方程式为:2Fe2++Cl2=2Fe3++2Cl-;
铁离子与硫氰根离子结合生成硫氰化铁,离子方程式为:Fe3++SCN-=[Fe(SCN)]2+ (或Fe3++3SCN-=Fe(SCN)3),
故答案为:稀盐酸(或稀硫酸溶液);2Fe2++Cl2=2Fe3++2Cl-;Fe3++SCN-=[Fe(SCN)]2+ (或Fe3++3SCN-=Fe(SCN)3);
(2)少量亚铁离子被空气中的氧气氧化成铁离子,所以加入KSCN溶液后,在未加新制氯水的情况下,溶液中也产生了红色,
故答案为:少量Fe2+被空气中氧气氧化成Fe3+.
点评:本题考查铁离子与亚铁离子的检验,难度中等.注意明确检验铁离子和亚铁离子的方法,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
已知有机物A与NaOH的醇溶液混合加热得产物C和溶液D.C与乙烯混合在催化剂作用下可反应生成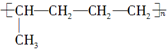 的高聚物.而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式可能为( )
的高聚物.而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式可能为( )
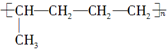 的高聚物.而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式可能为( )
的高聚物.而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式可能为( )A、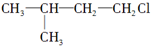 |
B、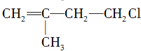 |
| C、CH3-CH2-CH2Cl |
D、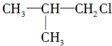 |
环境是人类生存和活动的场所.下列有关环境问题的说法不正确的是( )
| A、光化学烟雾的产生与汽车排放的尾气有关 |
| B、人们用电动自行车代替摩托车是“低碳消费”的行为 |
| C、酸雨是指PH小于7的酸性降水,主要是由煤的燃烧所致的 |
| D、用Cu、O2与稀H2SO4反应代替Cu与浓H2SO4反应制胆矾是“绿色化学”的体现 |
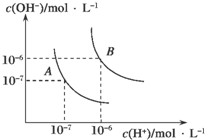 设反应①Fe(s)+CO2(g)?FeO(s)+CO(g)的平衡常数为K1.
设反应①Fe(s)+CO2(g)?FeO(s)+CO(g)的平衡常数为K1.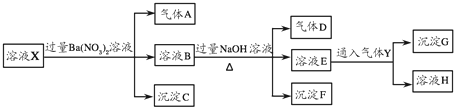
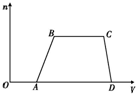 1L某混合溶液,可能含有的离子如下表:
1L某混合溶液,可能含有的离子如下表: