题目内容
下列有关铝及其化合物的叙述正确的是( )
| A、铝粉与氧化镁共热可制取金属镁 |
| B、足量铝分别与含1mol HCl、1mol NaOH的溶液反应,产生相同量的氢气 |
| C、在浓硝酸中加入等体积的浓硫酸后,立即加入铝片,铝片表面发生钝化 |
| D、工业上用电解熔融Al2O3的方法冶炼铝 |
考点:铝的化学性质,镁、铝的重要化合物
专题:元素及其化合物
分析:A.还原性Mg>Al,铝粉与氧化镁不反应;
B.2Al+2NaOH+2H2O═2NaAlO2+3H2↑、2Al+6HCl═2AlCl3+3H2↑,等量的酸、碱与足量Al反应,酸生成的气体少;
C.在浓硝酸中加入等体积的浓硫酸后,总体积变大,酸的浓度变小;
D.Al为活泼金属,利用电解法冶炼.
B.2Al+2NaOH+2H2O═2NaAlO2+3H2↑、2Al+6HCl═2AlCl3+3H2↑,等量的酸、碱与足量Al反应,酸生成的气体少;
C.在浓硝酸中加入等体积的浓硫酸后,总体积变大,酸的浓度变小;
D.Al为活泼金属,利用电解法冶炼.
解答:
解:A.还原性Mg>Al,铝粉与氧化镁不反应,MgO的熔点高,则电解氯化镁冶炼金属Mg,故A错误;
B.2Al+2NaOH+2H2O═2NaAlO2+3H2↑、2Al+6HCl═2AlCl3+3H2↑,等量的酸、碱与足量Al反应,酸生成的气体少,故B错误;
C.在浓硝酸中加入等体积的浓硫酸后,总体积变大,酸的浓度变小,则立即加入铝片,发生氧化还原反应,有气泡冒出,故C错误;
D.Al为活泼金属,氧化铝为离子化合物,则工业上用电解熔融Al2O3的方法冶炼铝,故D正确;
故选D.
B.2Al+2NaOH+2H2O═2NaAlO2+3H2↑、2Al+6HCl═2AlCl3+3H2↑,等量的酸、碱与足量Al反应,酸生成的气体少,故B错误;
C.在浓硝酸中加入等体积的浓硫酸后,总体积变大,酸的浓度变小,则立即加入铝片,发生氧化还原反应,有气泡冒出,故C错误;
D.Al为活泼金属,氧化铝为离子化合物,则工业上用电解熔融Al2O3的方法冶炼铝,故D正确;
故选D.
点评:本题考查物质的性质,为高频考点,综合考查元素化合物知识,把握物质的性质及发生的反应、金属冶炼等为解答的关键,侧重分析与知识综合应用能力的考查,题目难度不大.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
常温常压下,将a mol CO2气体通入1L bmol/L的NaOH溶液中,下列对所得溶液的描述不正确的是( )
A、当
| ||||||||
B、当a=b时,所得溶液中存在:c(OH-)+c(CO
| ||||||||
C、当
| ||||||||
D、当2a=b时,所得溶液中存在:c(Na+)>c(CO
|
已知有机物A与NaOH的醇溶液混合加热得产物C和溶液D.C与乙烯混合在催化剂作用下可反应生成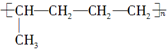 的高聚物.而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式可能为( )
的高聚物.而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式可能为( )
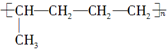 的高聚物.而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式可能为( )
的高聚物.而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式可能为( )A、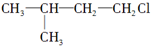 |
B、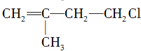 |
| C、CH3-CH2-CH2Cl |
D、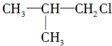 |
研究表明:多种海产品如虾、蟹、牡蛎等,体内含有+5价的砷(As)元素,但它对人体是无毒的,砒霜的成分是As2O3,属剧毒物质,专家忠告:吃饭时不要同时大量食用海鲜和青菜,否则容易中毒,并给出了一个公式:大量海鲜+大量维生素C=砒霜.下面有关解释不正确的应该是( )
| A、青菜中含有维生素C |
| B、维生素C具有还原性 |
| C、致人中毒过程中砷发生还原反应 |
| D、砒霜是氧化产物 |
镉镍可充电电池工作化学原理如下:Cd+2NiO(OH)+2H2O
Cd(OH)2+2Ni(OH)2,由此可知,该电池放电时的正极是( )
| 充电 |
| 放电 |
| A、Cd |
| B、NiO(OH) |
| C、Cd(OH)2 |
| D、Ni(OH)2 |
下列物质中,水解的最终产物含有葡萄糖的是( )
| A、油脂 | B、蛋白质 | C、蔗糖 | D、酶 |
环境是人类生存和活动的场所.下列有关环境问题的说法不正确的是( )
| A、光化学烟雾的产生与汽车排放的尾气有关 |
| B、人们用电动自行车代替摩托车是“低碳消费”的行为 |
| C、酸雨是指PH小于7的酸性降水,主要是由煤的燃烧所致的 |
| D、用Cu、O2与稀H2SO4反应代替Cu与浓H2SO4反应制胆矾是“绿色化学”的体现 |
 1L某混合溶液,可能含有的离子如下表:
1L某混合溶液,可能含有的离子如下表: