题目内容
【题目】高纯二氧化硅可用来制造光纤。某稻壳灰的成分为
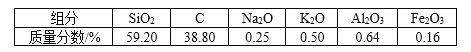
通过如下流程可由稻壳灰制备较纯净的二氧化硅。

请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中属于两性氧化物的是________。
(2)步骤①中涉及SiO2的离子反应方程式为______________。
(3)滤渣A的成分有________和_________(填化学式)。
(4)滤渣B的成分是________(填化学式)。
(5)过滤所需的玻璃仪器除烧杯和玻璃棒外,还有________。
【答案】Al2O3 SiO2 + 2 OH- = SiO32-+ H2O C Fe2O3 H2SiO3 漏斗
【解析】
稻壳灰用足量的氢氧化钠浸泡,稻壳灰中的C和Fe2O3不能被氢氧化钠容易溶解,因此过滤得A主要为硅酸钠溶液,含有少量的氢氧化钾和偏铝酸钠,滤渣A含有C以及氧化铁;硅酸钠溶液中加入盐酸生成硅酸沉淀,过滤、洗涤得滤渣B为硅酸,煅烧硅酸可得二氧化硅,据此分析解答。
(1)二氧化硅为酸性氧化物,氧化钠、氧化钾、氧化铁为碱性氧化物,氧化铝为两性氧化物,故答案为:Al2O3;
(2)二氧化硅为酸性氧化物,与氢氧化钠反应生成硅酸钠和水,离子方程式为:SiO2+2OH-═SiO32-+H2O,故答案为:SiO2+2OH-═SiO32-+H2O;
(3)氧化钠、氧化钾均能与水反应生成可溶性碱,氧化铝为两性氧化物能够与强碱反应生成可溶性偏铝酸盐,二氧化硅为酸性氧化物与氢氧化钠反应生成可溶性硅酸钠,三氧化二铁、碳与氢氧化钠不反应,所以过滤剩余的滤渣为C和Fe2O3,故答案为:C和Fe2O3。
(4)硅酸钠溶液中加入盐酸生成硅酸沉淀,过滤、洗涤得滤渣B为硅酸,故答案为:H2SiO3;
(5)过滤所需的玻璃仪器除烧杯和玻璃棒外,还需要漏斗,故答案为:漏斗。

 名校课堂系列答案
名校课堂系列答案