��Ŀ����
9���������ȡ����ͭ������ʾ��ͼ����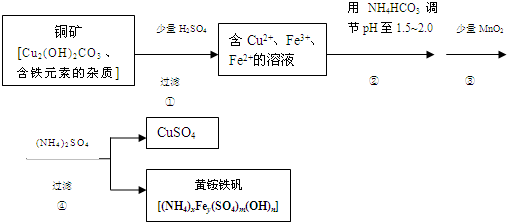
��1���������Cu2��OH��2CO3 ������Ӧ�Ļ�ѧ����ʽΪCu2��OH��2CO3+2H2SO4=2CuSO4+CO2��+3H2O��
��2���ڲ���۷����ķ�Ӧ�У�1mol MnO2ת��2mol ���ӣ��÷�Ӧ�����ӷ���ʽΪMnO2+2Fe2++4H+=Mn2++2Fe3++2H2O��
��3����С��Ϊ�ⶨ�����������ɣ�����������ʵ�飺
a����ȡ4.800g��Ʒ����������ȫ�ܽ�����100.00mL��ҺA��
b����ȡ25.00mL��ҺA������������KI����0.2500mol•L-1Na2S2O3��Һ���еζ�����Ӧ����ʽΪI2+2Na2S2O3=2NaI+Na2S4O6��������30.00mLNa2S2O3��Һ���յ㣮
b����ȡ25.00mL��ҺA������������NaOH��Һ��ַ�Ӧ���ˡ�ϴ�ӡ����յú�ɫ��ĩ0.600g��
c����ȡ25.00mL��ҺA��������BaCl2��Һ��ַ�Ӧ���ˡ�ϴ�ӡ�����ó���1.165g��
����Na2S2O3��Һ���еζ�ʱ���ζ����յ����ɫ�仯Ϊ�������һ��Na2S2O3��Һʱ����Һ��ɫǡ����ȥ���Ұ�����ڲ��ٻָ���ԭ����ɫ��
��ͨ������ȷ����������Ļ�ѧʽ��д��������̣���
���� ��1����ʽ̼��ͭ�����ᷴӦ��������ͭ��������̼��ˮ��
��2������������ǿ�����������Ժ��������ӷ���������ԭ��Ӧ���������ӱ�����Ϊ�����ӣ�
��3������Na2S2O3��Һ���еζ�ʱ���õ�����ָʾ��������Һ����ɫ��Ϊ��ɫ���Ұ������ɫ���ٱ仯˵���ζ������յ㣻
�ڲⶨ����������ԭ���ǣ�����⻯�غͻ��������������ӷ�Ӧ���ɵ��ʵ⣬�����������Ʒ�Ӧ��ͨ��������������Ƶ��������������������������Ȼ���������������������ᱵ������ͨ�����ᱵ������������������ӵ��������������غ�͵���غ���������Ӻ����������ӵ��������ݸ������ʵ���֮��д�����������Ļ�ѧʽ��
��� �⣺��1����ʽ̼��ͭ�����ᷴӦ�ķ���ʽֱ��д���ù۲취��ƽ��Cu2��OH��2CO3+2H2SO4=2CuSO4+CO2��+3H2O��
�ʴ�Ϊ��Cu2��OH��2CO3+2H2SO4=2CuSO4+CO2��+3H2O��
��2���������������ӱ���������ӣ�1mol MnO2ת�Ƶ���2 mol������Ԫ�ش�+4���+2�ۣ���Һ�������Եģ�����ʽ�����۲��Ҫ���������ӣ��ۺ�����������д�����ӷ���ʽΪMnO2+2Fe2++4H+=Mn2++2Fe3++2H2O��
�ʴ�Ϊ��MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O��
��2����Na2S2O3��Һ���еζ�ʱ���õ�����ָʾ�������������һ��Na2S2O3��Һʱ����Һ��ɫǡ����ȥ���Ұ�����ڲ��ٻָ���ԭ����ɫ��
�ʴ�Ϊ���������һ��Na2S2O3��Һʱ����Һ��ɫǡ����ȥ���Ұ�����ڲ��ٻָ���ԭ����ɫ��
��3���йصķ�Ӧ���ӷ���ʽΪ��2Fe3++2I-=2Fe2++I2��I2+2Na2S2O3=2NaI+Na2S4O6��
2Fe3+��I2��2Na2S2O3
n��Fe3+��=2n��I2��=n��Na2S2O3��=0.2500 mol•L-1��30.00 mL��10-3L•mL-1=7.50��10-3 mol��
��ȡ25.00mL��ҺA������������NaOH��Һ��ַ�Ӧ���ˡ�ϴ�ӡ����յú�ɫ��ĩFe2O30.600g������n��Fe3+��=2��Fe2O3��=2��0.600g/160g•mol-1=7.50��10-3 mol�������ڻ��������������+3�ۣ�
������BaCl2��Һ��ַ�Ӧ���ˡ�ϴ�ӡ������ó���1.165gΪ���ᱵ��������n��SO42-��=$\frac{1.165g}{233g/mol}$=5.00��10-3mol��
100 mL��Һ�к���n��Fe3+��=7.50��10-3 mol��$\frac{100mL}{25mL}$=0.03 mol��n��SO42-��=5.00��10-3 mol��$\frac{100mL}{25mL}$=0.02 mol��
��4.850g��Ʒ��笠����ӵ����ʵ���Ϊn��NH4+�����������������ʵ���Ϊn��OH-����
���������غ�ã�4.850g-0.03mol��56g/mol-0.02mol��96g/mol=n��NH4+����23g/mol+n��OH-����17g/mol
���ݵ���غ�ã�0.03mol��3+n��NH4+����1=0.02mol��2+n��OH-����1
��ã�n��NH4+��=0.01 mol��n��OH-��=0.06 mol��
x��y��m��n=n��NH4+����n��Fe3+����n��SO42-����n��OH-��=0.01��0.03��0.02��0.06=1��3��2��6��
��ѧʽΪNH4Fe3��SO4��2��OH��6��
�𣺻�������Ļ�ѧʽΪ��NH4Fe3��SO4��2��OH��6��
���� ���⿼���������ķ��롢�ᴿ��ʵ����ơ���ɵIJⶨ�ȣ��е��Ѷȣ�����ʱҪ���巴Ӧԭ����������������غ�͵���غ���������Ӻ����������ӵ����ʵ����ǽ���Ĺؼ���Ҫϸ�ļ��㣬ע���100mL��ȡ��25mL���еζ����γɳ��������׳�����

 ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д�
ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д� Сѧ������ҵϵ�д�
Сѧ������ҵϵ�д� ��ʿһ��ȫͨϵ�д�
��ʿһ��ȫͨϵ�д�| A�� | ���ܽ⡢���˵ķ�������̼��ƹ�����Ȼ��ƹ��� | |
| B�� | ���Ҵ���ȡ��ˮ�еĵ� | |
| C�� | ������ķ�����NaCl��Һ�з�������� | |
| D�� | �÷�Һ�ķ�������ֲ���ͺ�ˮ |

��֪������������������������ʽ����ʱ��Һ��pH���±���
| ������ | Fe��OH��3 | Fe��OH��2 | Al��OH��3 |
| ��ʼ���� | 2.3 | 7.5 | 3.4 |
| ��ȫ���� | 3.2 | 9.7 | 4.4 |
��1����������NaHCO3��Ŀ���ǵ���pH��4.4-7.5��Χ�ڣ�
��2����Ӧ���м���NaNO2��Ŀ���������������ӣ�д���÷�Ӧ�����ӷ���ʽΪ2H++Fe2++NO2-=Fe3++NO��+H2O��
��3����ʽ����������ˮ�����ɵ�Fe��OH��2+���ӿɲ���ˮ������Fe2��OH��42+�ۺ����ӣ���ˮ�ⷴӦ�����ӷ���ʽΪ2Fe��OH��2++2H2O?Fe2��OH��42++2H+��
��4����ҽҩ�ϳ����������������ᡢ����Ļ��Һ��Ӧ�Ʊ���ʽ�������������ҹ�����������Ʒ�в��ú���Fe2+��NO3-��Ϊ�������ò�Ʒ���Ƿ���Fe2+��Ӧʹ�õ��Լ�ΪD��
A����ˮ B��KSCN��Һ C��NaOH��Һ D������KMnO4��Һ
��5��Ϊ�ⶨ��Fe2+��Fe3+��Һ����Ԫ�ص��ܺ�����ʵ��������£�ȷ��ȡ20.00mL��Һ�ڴ�����ƿ�У���������H2O2������pH��2�����ȳ�ȥ����H2O2���������KI��ַ�Ӧ������ 0.1000mol•L-1 Na2S2O3����Һ�ζ����յ㣬���ı���Һ20.00mL��2Fe3++2I-�T2Fe2++I2 I2+2S2O3�T2I-+S4O62-��֪��
����Һ����Ԫ�ص��ܺ���Ϊ5.6g•L-1�����ζ�ǰ��Һ��H2O2û�г��������ⶨ����Ԫ�صĺ�������ƫ�� ���ƫ�ߡ���ƫ�͡������䡱��
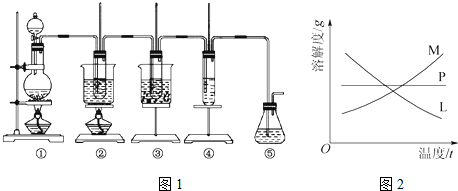
ͼ�У���Ϊ��������װ�ã��ڵ��Թ���ʢ��15mL 30%KOH��Һ����������ˮԡ�У��۵��Թ���ʢ��15mL8%NaOH��Һ�������ڱ�ˮԡ�У��ܵ��Թ��������ɫʯ����Һ����Ϊβ������װ�ã�
����д���пհף�
��1����ȡ����ʱ������ƿ�����һ�����Ķ������̣�ͨ����Һ©������д�������ƣ�����ƿ�м���������Ũ���ᣮʵ��ʱΪ�˳�ȥ�����е��Ȼ������壬���ڢ����֮�䰲װʢ��B������ĸ���ľ���װ�ã�
A����ʯ�ҡ������������� B������ʳ��ˮ
C��Ũ���� D������̼��������Һ
��2���Ƚ���ȡ����غʹ������Ƶ����������ߵIJ����Ǽ���Һ����Ӧ���Ũ�Ȳ�ͬ����Ӧ�¶Ȳ�ͬ��
��Ӧ��Ͼ���ȴ�ڵ��Թ����д�������������ͼ2�з��ϸþ����ܽ�����ߵ���M������ĸ�����Ӣڵ��Թ��з�����þ���ķ����ǹ��ˣ���ʵ��������ƣ���
��3����ʵ������ȡ�������Ƶ����ӷ���ʽ��Cl2+2OH-�TClO-+Cl-+H2O��
��4��ʵ���пɹ۲쵽�ܵ��Թ�����Һ����ɫ���������±仯������д�±��еĿհף�
| ʵ������ | ԭ�� |
| ��Һ��Ϊ��ɫ | ������ˮ��Ӧ���ɵ�H+ʹʯ���ɫ |
| �����Һ��Ϊ��ɫ | ������ˮ��Ӧ���ɵ�HClO��ʯ������Ϊ��ɫ���� |
| Ȼ����Һ����ɫ��Ϊ����ɫ | ����ͨ�����������ˮʹ��Һ�ʻ���ɫ |
 ��
��

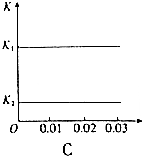
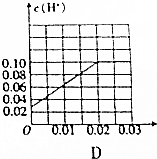


 ��1��װ�� I�е�Ũ����ܣ��ܻ��ܣ���ϡ������棬ԭ���Ƕ�������������ˮ���ʲ�����ϡ���ᣮ
��1��װ�� I�е�Ũ����ܣ��ܻ��ܣ���ϡ������棬ԭ���Ƕ�������������ˮ���ʲ�����ϡ���ᣮ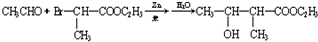 ��
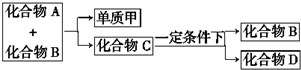
��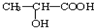 ͨ������·�߿ɺϳɣ�G����
ͨ������·�߿ɺϳɣ�G����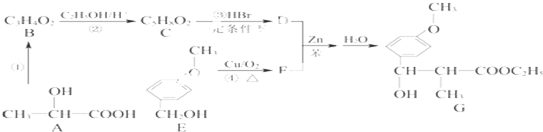
 ��
��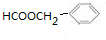 ��
��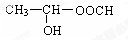 ��
��