题目内容
【题目】已知A→C必须加热,否则会发生钝化现象。请回答下列问题:
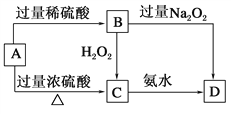
(1)A是________,你推断的理由是___________________。
(2)B在酸性条件下与H2O2反应的离子方程式:_____________________。
(3)A与过量浓H2SO4反应的化学方程式:_______________________。
【答案】 铁 A在浓硫酸中会钝化,且A与浓硫酸与稀硫酸反应的氧化产物不同 2H++2Fe2++H2O2===2H2O+2Fe3+ 6H2SO4(浓)+2Fe═Fe2(SO4)3+3SO2↑+6H2O
【解析】已知A→C必须加热,否则会发生钝化现象,则A为铁或铝,根据流程图,A与稀硫酸和浓硫酸反应生成不同的产物,其中B能够氧化生成C,则A为铁B为亚铁盐,C为铁盐。
(1) A在浓硫酸中会钝化,且A与浓硫酸与稀硫酸反应的氧化产物不同,因此A是铁,故答案为:铁;A在浓硫酸中会钝化,且A与浓硫酸与稀硫酸反应的氧化产物不同;
(2)硫酸亚铁在酸性条件下与H2O2反应被氧化为铁离子,反应的离子方程式为2H++2Fe2++H2O2===2H2O+2Fe3+,故答案为:2H++2Fe2++H2O2===2H2O+2Fe3+;
(3)铁与过量浓H2SO4反应生成硫酸铁、二氧化硫和水,反应的化学方程式为6H2SO4(浓)+2Fe═Fe2(SO4)3+3SO2↑+6H2O,故答案为:6H2SO4(浓)+2Fe═Fe2(SO4)3+3SO2↑+6H2O。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目