题目内容
【题目】I. 短周期元素X、Y、Z、W在周期表中的相对位置如图所示,其中W元素的原子结构示意图为 。
。
W | X | Y |
Z |
请回答下列问题:
(1)Z元素在元素周期表中的位置是__________________________________。
(2)X、Y、Z三种元素的原子半径由大到小的顺序为_________(元素符号表示)。
(3)X、Z、W三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序为________(用化学式表示)。
(4)用电子式表示WY2的形成过程__________________________________。
(5)写出W单质与浓硫酸反应的化学方程式_____________________________。
Ⅱ. A、B、C三种物质存在如图转化关系。
![]()
(6)若B为白色胶状不溶物,则A与C反应的离子方程式为_______________。
【答案】第三周期第VA族P>N>OHNO3>H3PO4>H2CO3![]() C+2H2SO4(浓)
C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2OAl3++3A1O2-+6H2O==4Al(OH)3↓
CO2↑+2SO2↑+2H2OAl3++3A1O2-+6H2O==4Al(OH)3↓
【解析】
I.根据W元素的原子结构示意图可知b=2,则a=6,即W是C,所以X是N,Z是P,Y是O,则
(1)P元素在元素周期表中的位置是第三周期第VA族。
(2)同周期自左向右原子半径逐渐减小,同主族从上到下原子半径逐渐增大,则X、Y、Z三种元素的原子半径由大到小的顺序为P>N>O。
(3)非金属性是N>P>C,非金属性越强,最高价含氧酸的酸性越强,因此X、Z、W三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序为HNO3>H3PO4>H2CO3。
(4)CO2是共价化合物,其形成过程可表示为![]() 。
。
(5)碳单质与浓硫酸反应的化学方程式为C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。
Ⅱ.(6)若B为白色胶状不溶物,则B是氢氧化铝,因此A与C是铝盐和偏铝酸盐,所以A与C反应的离子方程式为Al3++3A1O2-+6H2O=4Al(OH)3↓。

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案【题目】下图装置可用于收集气体并验证其化学性质,下列对应关系完全正确的是( )
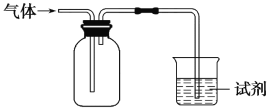
选项 | 气体 | 试剂 | 现象 | 结论 |
A | NO | 紫色石蕊溶液 | 溶液变红 | NO与水反应生成硝酸 |
B | Cl2 | 淀粉KI溶液 | 溶液变蓝 | Cl2有氧化性 |
C | SO2 | 品红溶液 | 溶液褪色 | SO2有强氧化性 |
D | NH3 | MgCl2溶液 | 产生白色沉淀 | NH3有碱性 |
A. AB. BC. CD. D