题目内容
【题目】(1)25℃时,将amolNH4NO3溶于水,溶液显酸性,原因是__(用离子方程式表示)。向该溶液中滴加bL氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将__(填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为__mol·L-1。(NH3·H2O的电离平衡常数为Kb=2×10-5)
(2)如图1是0.1mol/L电解质溶液的pH随温度变化的图像。
①其中符合0.1mol/LNH4Al(SO4)2溶液的pH随温度变化的曲线是__(填写字母),导致pH随温度变化的原因是__;
②20℃时,0.1mol/L的NH4Al(SO4)2溶液中2c(SO42-)-c(NH4+)-3c(Al3+)=___(填数值)。
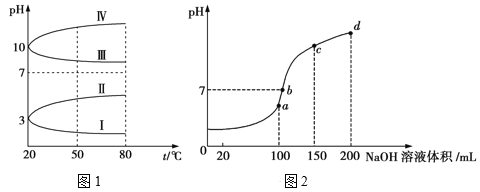
(3)室温时,向100mL0.1mol/L的NH4HSO4溶液中滴加0.1mol/LNaOH溶液,所得溶液的pH与所加NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是__;在b点,溶液中各离子浓度由大到小的排列顺序是__。
【答案】NH4++H2O![]() NH3·H2O+H+ 你像
NH3·H2O+H+ 你像 ![]() Ⅰ NH4Al(SO4)2溶液呈酸性,升高温度其水解程度增大,pH减小 10-3-10-11mol·L-1 a点 c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
Ⅰ NH4Al(SO4)2溶液呈酸性,升高温度其水解程度增大,pH减小 10-3-10-11mol·L-1 a点 c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
【解析】
(1)硝酸铵溶液中存在铵根离子的水解,NH4++H2O![]() NH3·H2O+H+,所以溶液显酸性;水解促进水的电离,酸或碱的电离抑制水的电离,所以随着氨水的滴入,水的电离平衡受到的促进作用减弱,即水的电离平衡逆向移动;NH3·H2O的电离平衡常数为Kb=
NH3·H2O+H+,所以溶液显酸性;水解促进水的电离,酸或碱的电离抑制水的电离,所以随着氨水的滴入,水的电离平衡受到的促进作用减弱,即水的电离平衡逆向移动;NH3·H2O的电离平衡常数为Kb=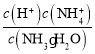 ,溶液中存在电荷守恒c(H+)+c(NH4+)=c(NO3-)+c(OH-),此时溶液呈中性,所以c(NH4+)=c(NO3-),设混合溶液的体积为V,则c(NH4+)=c(NO3-)=
,溶液中存在电荷守恒c(H+)+c(NH4+)=c(NO3-)+c(OH-),此时溶液呈中性,所以c(NH4+)=c(NO3-),设混合溶液的体积为V,则c(NH4+)=c(NO3-)=![]() mol/L,设氨水的浓度为x,溶液中存在物料守恒:c(NH4+)+ c(NH3·H2O)=
mol/L,设氨水的浓度为x,溶液中存在物料守恒:c(NH4+)+ c(NH3·H2O)=![]() mol/L,则混合溶液中c(NH3·H2O)=
mol/L,则混合溶液中c(NH3·H2O)=![]() mol/L-
mol/L-![]() mol/L=
mol/L=![]() mol/L,所以有
mol/L,所以有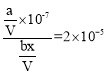 ,解得x=
,解得x=![]() mol/L;
mol/L;
(2)①NH4Al(SO4)2溶液中存在铵根和铝离子的水解,溶液呈酸性,升高温度其水解程度增大,pH减小,符合的曲线为Ⅰ;
②20℃时,0.1mol/L的NH4Al(SO4)2溶液pH=3,溶液中存在电荷守恒c(NH4+)-3c(Al3+)+c(H+)=2c(SO42-)+ c(OH-),所以2c(SO42-)-c(NH4+)-3c(Al3+)=c(H+)-c(OH-)=10-3 molL-1-10-11mol·L-1;
(3)a、b、c、d四个点,根据加入NaOH溶液的量可知a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4,b、c、d三点溶液均含有NH3H2O,(NH4)2SO4可以促进水的电离,而NH3H2O抑制水的电离,所以a点的水的电离程度最大;
b点溶液呈中性,溶液的溶质为(NH4)2SO4、Na2SO4、NH3H2O三种成分,a点时c(Na+)=c(SO

【题目】某学生以酚酞为指示剂用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液,三次实验分别记录有关数据如下表:
滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.100 0 mol·L-1盐酸的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
第一次 | 25.00 | 0.00 | 27.45 |
第二次 | 25.00 | 0.00 | 30.30 |
第三次 | 25.00 | 0.00 | 27.55 |
下列说法正确的是:
A. 当溶液从无色刚好变成红色时,则滴定终点达到
B. 该氢氧化钠溶液中c(NaOH)=0.110 0 mol·L-1
C. .滴定达终点时,滴定管尖嘴有悬液,则测定结果偏低
D. 实验中锥形瓶应用待测氢氧化钠溶液润洗
【题目】现用0.1000mol·L-1KMnO4酸性溶液滴定未知浓度的无色H2C2O4溶液,反应离子方程式是:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。
填空完成问题:
(1)该滴定实验所需的玻璃仪器有___。(填字母)
A.酸式滴定管 B.碱式滴定管 C.量筒 D.锥形瓶 E.铁架台 F.滴定管夹 G.烧杯 H.白纸 I.漏斗
(2)不用___(填“酸”或“碱”)式滴定管盛放高锰酸钾溶液。试分析原因__。
(3)滴定终点的现象为__。
(4)若滴定开始和结束时,滴定管中的液面如图所示,则起始读数为__mL,终点读数为__mL。
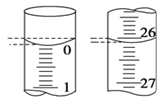
(5)某学生根据3次实验分别记录有关数据如下表:
滴定次数 | 待测H2C2O4溶液的体积/mL | 0.1000mol/LKMnO4的体积(mL) | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
依据上表数据列式计算该H2C2O4溶液的物质的量浓度为__。
(6)下列操作中可能使测定结果偏低的是__(填字母)。
A.酸式滴定管未用标准液润洗就直接注入KMnO4标准液
B.滴定前盛放草酸溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管尖嘴部分在滴定前没有气泡,滴定后有气泡
D.读取KMnO4标准液时,开始仰视读数,滴定结束时俯视读数
【题目】碳酸锶是重要的化工基础原料,由工业级硝酸锶(含有Ba2+、Ca2+、Mg2+等杂质)制备分析纯碳酸锶的工艺流程如下:
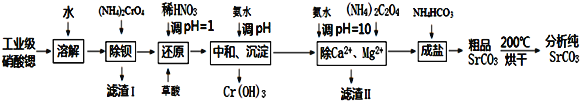
已知:①BaCrO4不溶于水,在水溶液中Cr2O72-与Ba2+不能结合。
②常温下,各物质的溶积常数如下表所示:
化合物 | Ca(OH)2 | CaC2O4 | Mg(OH)2 | MgC2O4 | Cr(OH)3 |
Ksp近似值 | 5.0×10-6 | 2.2×10-9 | 5.6×10-12 | 4.8×10-6 | 10-30 |
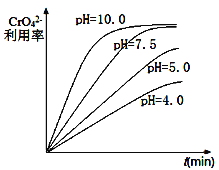
(1)“除钡”过程中CrO42-在不同pH时的利用率随时间变化曲线如下图所示,根据图像分析“除钡”过程中需要调节pH=7.5的原因_______________________________。
(2)“还原”过程中,应先调节pH=1.0,再加入草酸,加入草酸时发生反应的离子方程式为_____________________________。
(3)“滤渣Ⅱ”的主要成分为________________。
(4)“除Ca2+、Mg2+”后得到的滤液中除含有Sr(NO3)2外还含有过量的NH3·H2O,则“成盐”过程中发生反应的离子方程式为__________________________。
(5)“粗品SrCO3”烘干过程中除去的主要杂质为_____________________。
(6)在“中和、沉淀”步骤中,假定开始Cr3+,Zn3+浓度为0.1mol/L,调节至pH为_______时,铬开始沉淀;继续加碱调节至pH为_____时,铬刚好完全沉淀(离子浓度小于1×10-6mol/L时,即可认为该离子沉淀完全)。