题目内容
【题目】金属铝分别和O2、O3发生反应生成Al2O3 , 反应过程和能量关系如下图所示(图中的ΔH表示生成1 mol产物的数据)。下列有关说法中不正确的是( )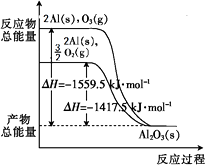
A.Al(s)与O3(g)反应的热化学方程式为2Al(s)+O3(g)=Al2O3(s) ΔH =-1559.5 kJ·mol-1
B.等质量的O2比O3的能量低
C.1 mol O2完全转化为O3 , 需吸收142 kJ的热量
D.给3O2(g) ![]() 2O3(g)的平衡体系加热,有利于O3的生成
2O3(g)的平衡体系加热,有利于O3的生成
【答案】C
【解析】A.根据图像, Al(s)与O3(g)反应的热化学方程式为2Al(s)+O3(g)=Al2O3(s) ΔH =-1559.5 kJ·mol-1 , A不符合题意;
B. 根据图像,2Al(s)+ ![]() O2(g)=Al2O3(s) ΔH =-1417.5 kJ·mol-1 , 结合A可知,
O2(g)=Al2O3(s) ΔH =-1417.5 kJ·mol-1 , 结合A可知, ![]() O2(g)
O2(g) ![]() O3(g) ΔH =+142 kJ·mol-1 , 等质量的O2比O3的能量低,B不符合题意;
O3(g) ΔH =+142 kJ·mol-1 , 等质量的O2比O3的能量低,B不符合题意;
C. 根据B的分析,1 mol O2完全转化为O3 , 需放出142 kJ的热量,C符合题意;
D. 3O2(g) ![]() 2O3(g)的正反应属于吸热反应,给平衡体系加热,温度升高,平衡正向移动,有利于O3的生成,D不符合题意;
2O3(g)的正反应属于吸热反应,给平衡体系加热,温度升高,平衡正向移动,有利于O3的生成,D不符合题意;
故答案为:CA.根据图像可直接得出反应ΔH 的值,从而得出该反应的热化学方程式;
B.根据图像,得出两个热化学方程式,根据盖斯定律,可确定 ![]() O2(g) O3(g)的ΔH , 从而确定O2和O3的能量大小;
O2(g) O3(g)的ΔH , 从而确定O2和O3的能量大小;
C.由C选项的分析,可知 ![]() O2(g) O3(g) ΔH =+142 kJ·mol-1;
O2(g) O3(g) ΔH =+142 kJ·mol-1;
D.反应为吸热反应,升高温度,平衡正移;

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目