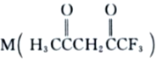题目内容
【题目】现有含有少量NaCl、Na2SO4、Na2CO3等杂质的NaNO3溶液,选择适当的试剂除去杂质,得到纯净的NaNO3固体,实验流程如下图所示。
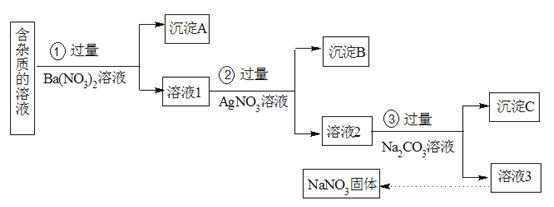
(1)沉淀A的主要成分是_________(填化学式)。
(2)②中反应的离子方程式是_________。
(3)③加入过量的Na2CO3溶液的目的是________。
(4)溶液3中肯定含有的杂质是_______,为除去杂质可向溶液3中加入过量的_______。
【答案】BaSO4、BaCO3 Cl-+Ag+=AgCl↓ 除去过量的Ba2+和Ag+ Na2CO3或CO32 稀硝酸
【解析】
由实验流程可知,在含有少量NaCl、Na2SO4、Na2CO3等杂质的NaNO3溶液中加入过量的Ba(NO3)2,反应生成BaSO4、BaCO3沉淀,过量得到的沉淀A中含有BaSO4、BaCO3;然后在溶液1中加入过量的AgNO3,使Cl-全部转化为AgCl沉淀,则沉淀B为AgCl;在溶液2中加入过量的Na2CO3,使溶液中的Ag+、Ba2+完全沉淀,最后所得溶液3为NaNO3和Na2CO3的混合溶液,可以加入稀HNO3,再蒸发得固体NaNO3,据此分析解答。
(1)根据上述分析,加入过量的Ba(NO3)2,Na2SO4、Na2CO3和Ba(NO3)2反应生成BaSO4、BaCO3沉淀,沉淀A的主要成分是BaSO4、BaCO3,故答案为:BaSO4、BaCO3;
(2)溶液1中含氯离子,加入过量的AgNO3,使Cl-全部转化为AgCl沉淀,反应的离子方程式为:Ag++Cl-═AgCl↓,故答案为:Ag++Cl-═AgCl↓;
(3)在所得溶液2中含有Ag+、Ba2+,在所得滤液中加入过量的Na2CO3,能够使溶液中的Ag+、Ba2+完全沉淀除去,故答案为:除去过量的Ba2+和Ag+;
(4)根据上述分析,溶液3为NaNO3和Na2CO3的混合溶液,含有的杂质为过量的Na2CO3,可以加入稀HNO3除去Na2CO3,经过蒸发浓缩、冷却结晶、过滤得到硝酸钠固体,故答案为:Na2CO3;HNO3。