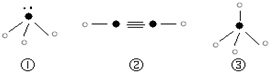
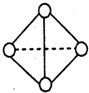
题目内容
已知:E为常见金属单质,C、D、F、I均为常见气体,其中C、D为单质,F、I为化合物,且组成元素相同,D、F有毒,I为直线型非极性分子,它们有如下框图关系: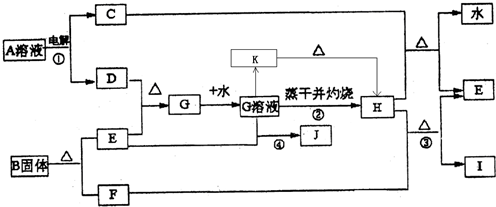
(1)反应①阳极的电极反应式______.
(2)反应③的化学方程式______.
(3)反应④的离子方程式为______.
(4)K是一种难溶于水的固体,K受热分解可生成H.实现由G溶液到K的转化时可以加入的试剂是(填写选项字母)______
A.NaOH溶液 B.氨水 C.Na2CO3溶液 D.NaHCO3溶液
(5)将G的饱和溶液加入到沸水中,继续加热可得红褐色液体,写出反应的离子方程式:______,该液体接通直流电后______极附近颜色加深,这种过程叫做______.
(6)若E中含有合金元素,会导致G不纯.测定G的质量分数通常可用碘量法测定:称取mg无水G样品,溶于稀盐酸,再转移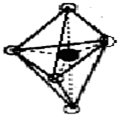 到
到
100mL容量瓶,用蒸馏水定容;取出10.00mL,加入稍过量的KI溶液,充分反应后,用淀粉作指示剂并用cmol?L-1Na2S2O3溶液滴定(I2+2S2O32-=2I-+S4O62-),共用去VmL.(杂质不参与反应)则样品中G的质量分数为:______.
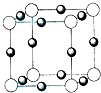
(7)B的结构为三角双锥(如图所示),图中○代表F分子,●代表E原子.则B的化学式为______.
解:由电解生成D并且有毒,则D应为氯气,I为直线型非极性分子,则应为CO2,F为CO,根据E与氯气反应后能继续与E反应,说明E是一种变价金属,应为Fe,则G为FeCl3,H为Fe2O3,J为FeCl2,C为H2,B分解生成Fe和CO,根据其结构模型可推知为Fe(CO)5,
(1)据题意,电解A溶液生成氢气和氯气,电解时阳极发生氧化反应,Cl-放电生成Cl2,电极反应式为2Cl--2e-=Cl2↑,
故答案为:2Cl--2e-=Cl2↑;
(2)工业炼铁是用还原性气体和CO在高温条件下发生氧化还原反应生成Fe,根据质量守恒定律可写出化学方程式为Fe2O3+3CO 2Fe+3CO2,
2Fe+3CO2,
故答案为:Fe2O3+3CO 2Fe+3CO2;
2Fe+3CO2;
(3)反应④为Fe3+和Fe发生氧化还原反应生成Fe2+,反应的离子方程式为2Fe3++Fe=3Fe2+,
故答案为:2Fe3++Fe=3Fe2+;
(4)K是一种难溶于水的固体,K受热分解可生成H,H为Fe2O3,则K应为Fe(OH)3,G为FeCl3,要生成Fe(OH)3,应加入碱或碱性溶液,题中ABCD都符合,
故答案为:ABCD;
(5)实验室制备Fe(OH)3胶体,可用沸水中滴加FeCl3溶液,FeCl3水解可生成Fe(OH)3胶体,反应的离子方程式为
FeCl3+3H2O(沸水)=Fe(OH)3(胶体)+3HCl,Fe(OH)3胶粒带正电荷,外加电源向阴极移动,此为胶体的电泳的性质,
故答案为:FeCl3+3H2O(沸水)=Fe(OH)3(胶体)+3HCl;阴极;电泳;
(6)涉及反应有2Fe3++2I-=2Fe2++I2,I2+2S2O32-=2I-+S4O62-,则可得关系式2Fe3+~I2~2S2O32-,
n(Na2S2O3)=V×10-3L×cmol/L=Vc×10-3mol,则10.00mL溶液中n(FeCl3)=Vc×10-3mol,
mg无水样品中n(FeCl3)=10×Vc×10-3mol=Vc×10-2mol,m(FeCl3)=Vc×10-2mol×162.5g/mol=1.625Vcg,
所以样品中ω(FeCl3)= =
= ,
,
故答案为: ;
;
(7)E为Fe,F为CO,由结构可知Fe和5个CO形成配位键,则分子式为Fe(CO)5或者FeC5O5,
故答案为:Fe(CO)5或者FeC5O5.
分析:由电解生成D并且有毒,则D应为氯气,I为直线型非极性分子,则应为CO2,F为CO,根据E与氯气反应后能继续与E反应,说明E是一种变价金属,应为Fe,则G为FeCl3,H为Fe2O3,J为FeCl2,C为H2,B分解生成Fe和CO,根据其结构模型可推知为Fe(CO)5;根据物质的性质结合质量守恒定律书写化学方程式和离子方程式;根据物质的性质完成实验操作.
点评:本题考查无机物的推断,并考查盐的水解、物质的制备等知识,具有一定的思维力度,做题时注意找出题目的关键点,牢固掌握物质的性质和实验基础知识.
(1)据题意,电解A溶液生成氢气和氯气,电解时阳极发生氧化反应,Cl-放电生成Cl2,电极反应式为2Cl--2e-=Cl2↑,
故答案为:2Cl--2e-=Cl2↑;
(2)工业炼铁是用还原性气体和CO在高温条件下发生氧化还原反应生成Fe,根据质量守恒定律可写出化学方程式为Fe2O3+3CO
 2Fe+3CO2,
2Fe+3CO2,故答案为:Fe2O3+3CO
 2Fe+3CO2;
2Fe+3CO2;(3)反应④为Fe3+和Fe发生氧化还原反应生成Fe2+,反应的离子方程式为2Fe3++Fe=3Fe2+,
故答案为:2Fe3++Fe=3Fe2+;
(4)K是一种难溶于水的固体,K受热分解可生成H,H为Fe2O3,则K应为Fe(OH)3,G为FeCl3,要生成Fe(OH)3,应加入碱或碱性溶液,题中ABCD都符合,
故答案为:ABCD;
(5)实验室制备Fe(OH)3胶体,可用沸水中滴加FeCl3溶液,FeCl3水解可生成Fe(OH)3胶体,反应的离子方程式为
FeCl3+3H2O(沸水)=Fe(OH)3(胶体)+3HCl,Fe(OH)3胶粒带正电荷,外加电源向阴极移动,此为胶体的电泳的性质,
故答案为:FeCl3+3H2O(沸水)=Fe(OH)3(胶体)+3HCl;阴极;电泳;
(6)涉及反应有2Fe3++2I-=2Fe2++I2,I2+2S2O32-=2I-+S4O62-,则可得关系式2Fe3+~I2~2S2O32-,
n(Na2S2O3)=V×10-3L×cmol/L=Vc×10-3mol,则10.00mL溶液中n(FeCl3)=Vc×10-3mol,
mg无水样品中n(FeCl3)=10×Vc×10-3mol=Vc×10-2mol,m(FeCl3)=Vc×10-2mol×162.5g/mol=1.625Vcg,
所以样品中ω(FeCl3)=
 =
= ,
,故答案为:
 ;
;(7)E为Fe,F为CO,由结构可知Fe和5个CO形成配位键,则分子式为Fe(CO)5或者FeC5O5,
故答案为:Fe(CO)5或者FeC5O5.
分析:由电解生成D并且有毒,则D应为氯气,I为直线型非极性分子,则应为CO2,F为CO,根据E与氯气反应后能继续与E反应,说明E是一种变价金属,应为Fe,则G为FeCl3,H为Fe2O3,J为FeCl2,C为H2,B分解生成Fe和CO,根据其结构模型可推知为Fe(CO)5;根据物质的性质结合质量守恒定律书写化学方程式和离子方程式;根据物质的性质完成实验操作.
点评:本题考查无机物的推断,并考查盐的水解、物质的制备等知识,具有一定的思维力度,做题时注意找出题目的关键点,牢固掌握物质的性质和实验基础知识.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
 (2011?平顶山二模)A、B、C、D、E五种前四周期元素,原子序数依次增大.已知D元素原子核外的M层上有3个单电子存在.在周期表中,B、E与D同主族,A、C分别与B、D处于相邻位置.回答下列问题:
(2011?平顶山二模)A、B、C、D、E五种前四周期元素,原子序数依次增大.已知D元素原子核外的M层上有3个单电子存在.在周期表中,B、E与D同主族,A、C分别与B、D处于相邻位置.回答下列问题: ”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示上述相关元素的原子中除去最外层电子的剩余部分,“ ”表示氢原子,小黑点“
”表示氢原子,小黑点“