题目内容
【题目】下列有关钠及其化合物的有关说法中正确的是( )
A.钠与CuSO4溶液反应的离子方程式为2Na+Cu2+═Cu+2Na+
B.7.8 g Na2O2含离子数为0.4NA
C.“侯氏制碱法”中的碱指NaHCO3
D.向Na2CO3饱和溶液中通入足量的CO2,有NaHCO3结晶析出
【答案】D
【解析】
A. 将金属钠放入CuSO4溶液中,钠先与水反应生成NaOH,NaOH再与CuSO4反应;
B. 1molNa2O2中存在2molNa+和1molO22-;
C. “侯氏制碱法”中的碱为Na2CO3
D. 相同条件下NaHCO3的溶解度小于Na2CO3的溶解度。
A. 钠与硫酸铜溶液反应,生成氢氧化铜沉淀、硫酸钠和氢气,离子方程式:Cu2++2Na+2H2O=Cu(OH)2↓+2Na++H2↑,A项错误;
B. 7.8 g Na2O2物质的量为:![]() =0.1mol,含有0.2mol Na+,0.1mol O22-,共含离子数为0.3NA,B项错误;
=0.1mol,含有0.2mol Na+,0.1mol O22-,共含离子数为0.3NA,B项错误;
C. “侯氏制碱法”中的碱为Na2CO3,C项错误;
D. Na2CO3+H2O+CO2=2NaHCO3,相同条件下NaHCO3的溶解度小于Na2CO3的溶解度,因此向Na2CO3饱和溶液中通入CO2,有NaHCO3结晶析出,D项正确;
答案选D。
生成气体型 | 钠与NH4Cl溶液反应生成H2和NH3 |
生成沉淀型 | 钠与铜盐、铁盐等溶液反应生成Cu(OH)2或Fe(OH)3 |
复杂型 | 钠与AlCl3稀溶液反应,如果钠量较多,则先生成Al(OH)3沉淀,后沉淀溶解 |

 口算能手系列答案
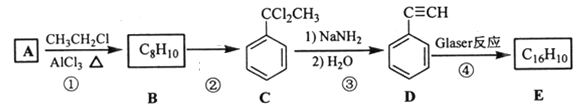
口算能手系列答案【题目】草酸钴可用于指示剂和催化剂的制备。用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)制取CoC2O4·2H2O工艺流程如下

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
完全沉淀的pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
(1)CoC2O4·2H2O中C的化合价是____________________________。
(2)写出浸出过程中Na2SO3与Co2O3发生反应的离子方程式:______________。
(3)浸出液中加入NaClO3的目的是____________________________。
(4)加Na2CO3能使浸出液中某些金属离子转化成氢氧化物沉淀,沉淀除Al(OH)3外,还有的成分是______________(填化学式),试用离子方程式和必要的文字简述其原理:____________________________。
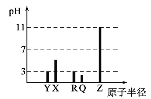
(5)萃取剂对金属离子的萃取率与pH的关系如图,萃取剂的作用是______________;其使用的适宜pH范围是______________。

A. 2.02.5
B. 3.03.5
C. 4.04.5
(6)滤液I“除钙、镁”是将其转化为MgF2、CaF2沉淀。己知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,当加入过量 NaF后,所得滤液 c(Mg2+)/c(Ca2+) =______________。
(7)用m1kg水钴矿(含Co2O360%)制备CoC2O4·2H2O,最终得到产品m2kg,产率(实际产量/理论产量×100%)为____________________________。(已知:M(Co2O3)=166, M(CoC2O4·2H2O)=183,仅需列出数字计算式)。
【题目】NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+=Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况。
(1)此消毒液中NaClO可吸收空气中的CO2生成NaHCO3和HClO。写出化学反应方程式___。
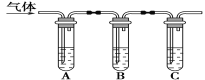
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出。通过以下装置检验气体的成分可以判断消毒液是否变质。
限选试剂:98%浓硫酸、1%品红溶液、1.0mol·L-1KI淀粉溶液、1.0mol·L-1NaOH溶液、澄清石灰水、饱和NaCl溶液。
请完成下列实验方案。
所加试剂 | 预期现象和结论 |
试管A中加足量①___; 试管B中加1%品红溶液; 试管C中加②___。 | 若A中溶液变蓝色,B中溶液不褪色,C中溶液变浑浊,则消毒液部分变质;③___,则消毒液未变质;④___,则消毒液完全变质。 |