题目内容
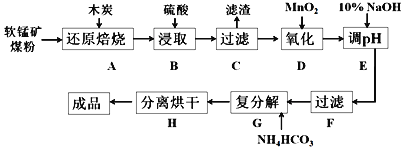
【题目】高纯MnCO3在电子工业中有重要的应用,工业上利用软锰矿(主要成分是MnO2,还含有Fe2O3、CaCO3、CuO等杂质)制取碳酸锰的流程如图所示:
已知:还原焙烧主反应为2MnO2+C![]() 2MnO+CO2↑。
2MnO+CO2↑。
可能用到的数据如下:

根据要求回答下列问题:
(1)在实验室进行步骤A,混合物应放在__________中加热;步骤C中的滤渣为__________。
(2)步骤D中氧化剂与还原剂的物质的量之比为__________。
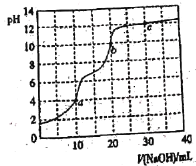
(3)步骤E中调节pH的范围为____________,其目的是______________________________。
(4)步骤G,温度控制在35℃以下的原因是____________________________________,若Mn2+恰好沉淀完全时测得溶液中CO32-的浓度为2.2×10-6mol/L,则Ksp(MnCO3)=____________。
(5)生成的MnCO3沉淀需经充分洗涤,检验洗涤是否干净的方法是_____________________。
(6)现用滴定法测定产品中锰元素的含量。实验步骤:称取3.300 g试样,向其中加入稍过量的磷酸和硝酸,加热使产品中MnCO3完全转化为[Mn(PO4)2]3-(其中NO3-完全转化为NO2-);加入稍过量的硫酸铵,发生反应NO2-+NH4+=N2↑+2H2O以除去NO2-;加入稀硫酸酸化,再加入60.00 mL 0.500 mol·L-1硫酸亚铁铵溶液,发生的反应为[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2PO43-;用5.00 mL 0.500 mol·L-1酸性K2Cr2O7溶液恰好除去过量的Fe2+。
①酸性K2Cr2O7溶液与Fe2+反应的离子方程式为_____________________________________。
②试样中锰元素的质量分数为____________。
【答案】坩埚 C、 Cu和CaSO4 1∶2 3.7≤pH<8.1 使Fe3+转化为Fe(OH)3而除去,而不影响Mn2+ 减少碳酸氢铵的分解,提高原料利用率 2.2×10-11 取少量最后一次的洗涤液于试管中,向其中滴加用盐酸酸化的BaCl2溶液,若无白色沉淀产生,则表明已洗涤干净 6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O 25%
【解析】
(1)~(5)原料加木炭焙烧,主要发生2MnO2+C![]() 2MnO+CO2↑,且C与Fe2O3、CuO发生反应,生成Fe、Cu,再用硫酸酸浸过滤得到MnSO4、FeSO4溶液,过滤分离出滤渣为不和稀硫酸反应的Cu、过量的木炭以及碳酸钙转化成的CaSO4,再氧化、调节pH除去Fe3+得到MnSO4溶液,最后与NH4HCO3反应生成MnCO3,分离烘干得到MnCO3,以此来解答。
2MnO+CO2↑,且C与Fe2O3、CuO发生反应,生成Fe、Cu,再用硫酸酸浸过滤得到MnSO4、FeSO4溶液,过滤分离出滤渣为不和稀硫酸反应的Cu、过量的木炭以及碳酸钙转化成的CaSO4,再氧化、调节pH除去Fe3+得到MnSO4溶液,最后与NH4HCO3反应生成MnCO3,分离烘干得到MnCO3,以此来解答。
(6)滴定原理为:利用酸性K2Cr2O7滴定剩余的Fe2+的量,从而确定与[Mn(PO4)2]3-反应的Fe2+的量,继而确定Mn元素的量。
(1)高温焙烧物质应在坩埚中进行;根据分析可知滤渣为C、Cu和CaSO4;
(2)步骤D中MnO2被还原成Mn2+,化合价降低2价,Fe2+被氧化成Fe3+,化合价升高1价,根据得失电子守恒,氧化剂与还原剂的物质的量之比为1:2;
(3)此时溶液中的杂质主要为Fe3+,结合表中数据可知步骤E中调节pH的范围为3.7≤pH<8.3,其目的是使铁离子转化为氢氧化铁而除去,而不影响Mn2+;
(4)铵盐不稳定,受热易分解,所以步骤G中温度需控制在35℃以下,减少碳酸氢铵的分解,提高原料利用率;Mn2+恰好沉淀完全时可认为c(Mn2+)=10-5mol/L,Ksp(MnCO3)= c(Mn2+)·c(CO32-)=10-5×2.2×10-6=2.2×10-11;
(5)生成的MnCO3沉淀可能附着有硫酸盐,所以检验是否含有硫酸根即可确认沉淀是否洗涤干净,具体操作为:取少量最后一次的洗涤液于试管中,向其中滴加用盐酸酸化的BaCl2溶液,若无白色沉淀产生,则表明已洗涤干净;
(6)①酸性K2Cr2O7具有强氧化性,可以把亚铁离子氧化成铁离子,自身被还原成Cr3+,根据电子守恒、电荷守恒和原子守恒可得离子方程式为6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O;
②根据方程式6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O可知剩余n(Fe2+)= 0.500 mol·L-1×0.005L×6=0.015mol,则与[Mn(PO4)2]3-反应的n(Fe2+)=0.500 mol·L-1×0.06L-0.015mol=0.015mol,根据方程式[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2PO43-可知n(Mn)=0.015mol,所以锰元素的质量分数为![]() =25%。
=25%。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案