题目内容
1.下列关于Na和 Na+的叙述中,错误的是( )| A. | 它们相差一个电子层 | B. | 它们都有强还原性 | ||
| C. | 钠原子、钠离子均为同一元素 | D. | 灼烧时,它们的焰色反应都呈黄色 |
分析 Na+是钠原子失去一个电子后形成的,有2个电子层,根据钠原子和钠离子的结构来分析稳定性和化学性质,根据它们的质子和电子来分析它们的转化及是否为同种元素.
解答 解:A.Na+是钠原子失去一个电子后形成的,有2个电子层,而钠原子有3个电子层,所以它们相差一个电子层,故A正确;
B.Na+化合价不能升高,无还原性,故B错误;
C.Na+是钠原子失去一个电子后形成的,质子数没有改变,所以钠原子、钠离子均为同一元素,故C正确;
D.Na+是钠原子失去一个电子后形成的,质子数没有改变,所以钠原子、钠离子均为同一元素,都是钠元素,所以灼烧时,它们的焰色反应都呈黄色,故D正确.
故选B.
点评 本题考查原子和离子的转化及它们的性质的分析,难度不大,学生应能从微粒的结构的角度来分析,明确最外层8电子是稳定结构来分析性质.

练习册系列答案
 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
12.如果你家里的食用豆油混有一些水,你将采用下列何种方法分离( )
| A. | 过滤 | B. | 分液 | C. | 萃取 | D. | 蒸馏 |
16.已知:H2(g)+F2(g)═2HF(g)△H=-270kJ•mol-1,下列说法不正确的是( )
| A. | 44.8 L氟化氢气体分解成22.4 L的氢气和22.4 L的氟气吸收270 kJ热量 | |
| B. | 1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量大于270 kJ | |
| C. | 相同条件下,1 mol氢气与1 mol氟气的能量总和高于2 mol氟化氢气体的能量 | |
| D. | 2 mol H-F键的键能比1 mol H-H键和1 mol F-F键的键能之和大270 kJ |
6.下列各组混合物中,能用分液漏斗进行分离的是( )
| A. | 酒精和水 | B. | 溴和CCl4 | C. | 水和苯 | D. | 汽油和植物油 |
13.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 为防止中秋月饼等富脂等食品被氧化,常在包装中放入还原铁粉等 | |
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率,属于牺牲阴极的阳极保护法 | |
| C. | 镀层破坏后,镀锡铁板比镀锌铁板更易腐蚀 | |
| D. | 电解熔融MgCl2,可制得金属镁 |
10.下列表示对应化学反应的离子方程式或化学方程式正确的是( )
| A. | 向NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全: NH4++H++SO42-+Ba2++2OH-=NH3•H2O+BaSO4↓+H2O | |
| B. | Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O | |
| C. | 用铜作电极电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| D. | 以下有机物在碱性条件下水解的化学方程式: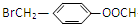 +3NaOH$\stackrel{△}{→}$ +3NaOH$\stackrel{△}{→}$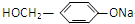 +HCOONa+NaBr +HCOONa+NaBr |
11.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A. | 标准状况下,2.24LCHCl3的原子总数为0.1NA | |
| B. | 1mol甲基(-CH3)所含的电子总数为9 NA | |
| C. | 1mol•L-1的醋酸钠溶液中含有的CH3COO-数目为NA | |
| D. | 60g二氧化硅晶体中含有Si-O键数目为2NA |
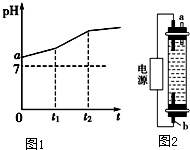 用惰性电极电解物质的量比为2:1的NaCl与NaHCO3混合溶液,溶液pH变化如图1所示.
用惰性电极电解物质的量比为2:1的NaCl与NaHCO3混合溶液,溶液pH变化如图1所示.