题目内容
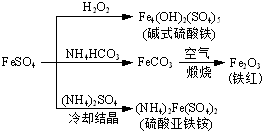
电子工业中常用FeCl3溶液腐蚀覆铜板来制作印刷电路板,并回收Cu和综合利用FeCl3溶液.流程图如图所示:

请回答:
(1)试剂A是______.
(2)过程①反应的离子方程式是______.
(3)过程③反应的离子方程式是______.
(4)检验废液中Fe3+存在的方法是______.
(5)若在10g滤渣中加入足量盐酸,放出1.12LH2(标准状况),则滤渣中Cu的质量分数是______.

请回答:
(1)试剂A是______.
(2)过程①反应的离子方程式是______.
(3)过程③反应的离子方程式是______.
(4)检验废液中Fe3+存在的方法是______.
(5)若在10g滤渣中加入足量盐酸,放出1.12LH2(标准状况),则滤渣中Cu的质量分数是______.
(1)废液中铜石以Cu2+形式存在的,要回收Cu应当选合适的还原剂还原,根据题意,应选铁粉,故答案为:铁粉;
(2)过程①是FeCl3溶液与铜反应,反应离子方程式为:2Fe3++Cu=2Fe2++Cu2+,故答案为;2Fe3++Cu=2Fe2++Cu2+;
(3)过程③是把滤液中的Fe2+再氧化为Fe3+;故需要加入氯气,反应离子方程式为:2Fe2++Cl2=2Cl-+2Fe3+,故答案为:2Fe2++Cl2=2Cl-+2Fe3+;
(4)检验Fe3+常用KSCN溶液,故答案为:取少量废液与试管中,滴加KSCN溶液,若溶液变红色,说明废液中含有Fe3+;
(5)n(H2)=
=
=0.05mol,再由方程式:Fe+2H+=Fe2++H2↑,可求得n(Fe)=0.05mol,则m(Fe)=n?M=2.8g,故m(Cu)=7.2g,所以则滤渣中Cu的质量分数=
×100%=72%,故答案为72%.
(2)过程①是FeCl3溶液与铜反应,反应离子方程式为:2Fe3++Cu=2Fe2++Cu2+,故答案为;2Fe3++Cu=2Fe2++Cu2+;
(3)过程③是把滤液中的Fe2+再氧化为Fe3+;故需要加入氯气,反应离子方程式为:2Fe2++Cl2=2Cl-+2Fe3+,故答案为:2Fe2++Cl2=2Cl-+2Fe3+;
(4)检验Fe3+常用KSCN溶液,故答案为:取少量废液与试管中,滴加KSCN溶液,若溶液变红色,说明废液中含有Fe3+;
(5)n(H2)=
| v |
| Vm |
| 1.12L |
| 22.4L/mol |
| 7.2 |
| 10 |

练习册系列答案
相关题目