题目内容
19.在容积为2L的密闭容器中进行如下反应:A(g)+2B(g)?3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol•L-1•min-1.计算:
(1)5min末A的物质的量浓度为1.5 mol/L.
(2)前5min内用B表示的化学反应速率v(B)为0.2 mol/(L•min).
(3)化学方程式中n值为2.
(4)此反应在四种不同情况下的反应速率分别为:
①v(A)=5mol•L-1•min-1
②v(B)=6mol•L-1•min-1
③v(C)=4.5mol•L-1•min-1
④v(D)=8mol•L-1•min-1
其中反应速率最快的是①(填编号).
分析 (1)根据C的物质的量计算反应的A的物质的量,从而知道为反应的A的物质的量,再利用浓度公式 计算;
(2)根据C的物质的量计算反应的B的物质的量,根据反应速率公式计算;
(3)根据同一反应中、同一时间段内,各物质的反应速率之比等于计量数之比确定n值;
(4)把不同物质的反应速率换算成同一物质的反应速率进行比较.
解答 解:(1)A(g)+2B(g)?3C(g)+nD(g),
反应开始 4mol 6mol 0 0
反应 1 mol 2 mol 3 mol
5min末 3 mol 4mol 3 mol
C(A)=$\frac{n}{V}$=1.5 mol/L
故答案为:1.5 mol/L;
(2)v(B)=$\frac{△n}{V△t}$=$\frac{2}{2×5}$=0.2 mol/(L•min)
故答案为:0.2 mol/(L•min);
(3)根据同一反应中、同一时间段内,各物质的反应速率之比等于计量数之比;
所以v(B):v(D)=0.2 mol/(L•min):0.2mol/(L•min)=2:n,n=2
故答案为:2;
(4)把所有速率都换算成A的反应速率;
①v(A )=5mol/( L•min )
②由v( B )=6 mol/( L•min )知,v(A )=3mol/( L•min )
③由v(C)=4.5mol/( L•min )知,v(A )=1.5 mol/( L•min )
④由v(D )=8mol/( L•min )知,v(A )=4mol/( L•min )
故选:①.
点评 本题考查了化学平衡计算分析,反应速率、浓度的计算应用,掌握基础是关键,题目较简单,解答(4)的方法是:把所有速率都换算成同一物质的反应速率,然后比较大小,从而确定反应速率快慢.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.H-H键的键能是436kJ•mol -1,Br-Br键的键能是194kJ•mol -1,H-Br键的键能是356kJ•mol -1.则对反应H2(g)+Br2(g)?2HBr(g)的说法,不正确的是( )
| A. | 吸热反应 | B. | 放热反应 | C. | 化合反应 | D. | 可逆反应 |
4.二氧化硅是酸性氧化物是因为( )
| A. | 硅是非金属 | |
| B. | 它是非金属氧化物 | |
| C. | 二氧化硅能跟氢氧化钠反应生成盐和水 | |
| D. | 它的对应水化物是弱酸,能溶于水 |
11.下列叙述正确的是( )
| A. | Fe分别与氯气和稀盐酸反应所得氯化物相同 | |
| B. | K、Zn分别与不足量的稀硫酸反应所得溶液均呈中性 | |
| C. | C、P、S、Cl的最高价氧化物对应水化物的酸性逐渐增强 | |
| D. | Li、Na、K的原子半径和密度随原子序数的增加而增大 |
8.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 100 mL 0.1 mol•L-1 Na2SO4溶液中,粒子总数是0.03NA | |
| B. | 常温常压下,32 g O2-中所含电子的数目为17NA | |
| C. | 1 mol Al3+完全水解生成氢氧化铝胶体粒子的数目为NA | |
| D. | 标准状况下,分子数为NA的N2、C2H4混合气体的质量无法确定 |
9.下列反应的离子方程式正确的是( )
| A. | 次氯酸钙溶液中通入过量二氧化碳 Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO | |
| B. | 硫酸亚铁溶液中加过氧化氢溶液 Fe2++2H2O2+4H+═Fe3++4H2O | |
| C. | Fe2(SO4)3的酸性溶液中通入足量硫化氢 Fe3++H2S═Fe2++S↓+2H+ | |
| D. | 氯化亚铁溶液中加入稀硝酸 3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ |
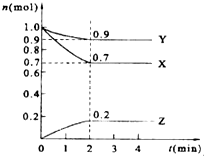 某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.