题目内容
氯碱工业的产物NaOH与不同物质反应可以生成不同的盐。已知常温下,浓度均为
0.1 mol·L-1的4种钠盐溶液的pH如下表:
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.2 |
下列说法中正确的是( )
A.向氯水中加入NaHCO3溶液,可以增大氯水中次氯酸的浓度
B.四种溶液中,水的电离程度最大的是NaClO
C.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO溶液,pH最大的是H2SO3溶液
D.NaHSO3溶液中离子浓度大小顺序为c(Na+)>c(H+)>c(HS
 )>c(S
)>c(S )>c(OH-)
)>c(OH-)
A
解析试题分析:不同的弱酸与同种碱发生反应得到的盐的水溶液的pH关系是:酸越强,盐溶液的pH就越小,酸越弱,相应的盐溶液的pH就越大。A.向氯水中加入NaHCO3溶液,由于在氯水中存在平衡:Cl2+H2O HCl+HClO,由于酸性HCl> H2CO3> HClO,所以会发生反应NaHCO3+HCl=NaCl+H2O+ CO2↑,使Cl2+H2O
HCl+HClO,由于酸性HCl> H2CO3> HClO,所以会发生反应NaHCO3+HCl=NaCl+H2O+ CO2↑,使Cl2+H2O HCl+HClO正向移动,c(HClO)增大。正确。B.在四种溶液中,由于Na2CO3的pH最大,所以水的电离程度最大的是Na2CO3。错误。C.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO溶液,电离程度最大的是H2SO3。酸的电离程度越大,c(H+)越大,溶液的pH越小。所以pH最大的是HClO溶液.错误。D.在NaHSO3溶液中,存在电离:NaHSO3=Na++ HSO3-,电离平衡:HSO3-
HCl+HClO正向移动,c(HClO)增大。正确。B.在四种溶液中,由于Na2CO3的pH最大,所以水的电离程度最大的是Na2CO3。错误。C.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO溶液,电离程度最大的是H2SO3。酸的电离程度越大,c(H+)越大,溶液的pH越小。所以pH最大的是HClO溶液.错误。D.在NaHSO3溶液中,存在电离:NaHSO3=Na++ HSO3-,电离平衡:HSO3- H++ SO32-。水解平衡:HSO3-+H2O
H++ SO32-。水解平衡:HSO3-+H2O OH-+ H2SO3。由于在NaHSO3溶液中,pH=5.2.说明HSO3-的电离作用大于水解作用。但是盐的电离作用大于弱电解质的电离作用,所以在此溶液中各种离子浓度大小顺序为c(Na+)> c(HSO3-)> c(H+)>c(SO32-)>c(OH-)。错误。
OH-+ H2SO3。由于在NaHSO3溶液中,pH=5.2.说明HSO3-的电离作用大于水解作用。但是盐的电离作用大于弱电解质的电离作用,所以在此溶液中各种离子浓度大小顺序为c(Na+)> c(HSO3-)> c(H+)>c(SO32-)>c(OH-)。错误。
考点:考查弱酸盐溶液的pH在比较离子浓度的大小、反应的进行、溶液酸碱性的应用的知识。

 黄冈创优卷系列答案
黄冈创优卷系列答案下列液体均处于25 ℃,有关叙述正确的是( )。
| A.某物质溶液的pH>7,则该物质一定是碱或强碱弱酸盐 |
| B.pH=6.5的牛奶中c(H+)是pH=4.5的H2SO4溶液中c(H+)的100倍 |
| C.pH=3的醋酸与pH=11的NaOH溶液等体积混合后溶液中: c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D.AgCl在等浓度的CaCl2溶液和NaCl溶液中的溶解度相同 |
下列说法正确的是
| A.向50 mL 1 mol·L-1的盐酸中加入烧碱,水的KW不变 |
| B.NH4Cl和NH3·H2O混合液中,二者对对方的平衡都起了抑制作用 |
| C.有两种弱酸HX和HY且酸性HX>HY,则体积和浓度相同的NaX和NaY溶液中有c(Y-)>c(X-)>c(OH-)>c(H+) |
D.常温下0.1 mol·L-1的HA溶液中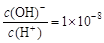 , 则0.01 mol·L-1HA溶液中c(H+)=1×10-4 mol·L-1 , 则0.01 mol·L-1HA溶液中c(H+)=1×10-4 mol·L-1 |
用水稀释0.1mol· L-1的醋酸溶液,下列说法正确的是( )
| A.醋酸的电离程度逐渐增大,溶液的PH值减小 |
| B.水的电离程度增大 |
| C.Kw逐渐减小 |
D. 变大 变大 |
下列说法正确的是
| A.水的离子积常数KW只与温度有关,但外加酸、碱、盐一定会影响水的电离程度 |
| B.Ksp不仅与难溶电解质的性质和温度有关,还与溶液中相关离子的浓度有关 |
C.常温下,在0.10 mol·L-1的NH3·H2O溶液中加入少量NH4Cl晶体,能使溶液的pH减小,c(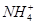 )/c(NH3·H2O)的值增大 )/c(NH3·H2O)的值增大 |
| D.室温下,CH3COOH的KW=1.7×10-5,NH3·H2O的Kb=1.7×10-5,CH3COOH溶液中的c(H+)与NH3·H2O中的c(OH-)相等 |
在t ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知t ℃时AgCl的Ksp=4×10-10,下列说法不正确的是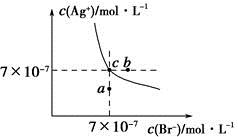
| A.在t ℃时,AgBr的Ksp为4.9×10-13 |
| B.在AgBr饱和溶液中加入NaBr固体,可使溶液由c点变到b点 |
| C.图中a点对应的是AgBr的不饱和溶液 |
D.在t ℃时,AgCl(s)+Br-(aq) AgBr(s)+Cl-(aq)平衡常数K≈816 AgBr(s)+Cl-(aq)平衡常数K≈816 |
氨水中存在下列的电离平衡:NH3·H2O NH
NH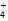 +OH-要使平衡向左移动,同时使OH-离子浓度增大,应加入下列的( )
+OH-要使平衡向左移动,同时使OH-离子浓度增大,应加入下列的( )
| A.NaOH固体 | B.NH4Cl固体 |
| C.H2SO4 | D.H2O |
常温下,将0.1 mol·L-1氢氧化钠溶液与0.06 mol·L-1硫酸溶液等体积混合,该混合溶液的pH等于( )
| A.1.7 | B.2.0 | C.12.0 | D.12.4 |
溶度积常数表达式符合Ksp=·c(By-)的是( )
A.AgCl(s) Ag+(aq)+Cl-(aq) Ag+(aq)+Cl-(aq) |
B.Na2S 2Na++S2- 2Na++S2- |
C.Ag2S(s) 2Ag+(aq)+S2-(aq) 2Ag+(aq)+S2-(aq) |
D.PbI2(s) Pb2+(aq)+2I-(aq) Pb2+(aq)+2I-(aq) |