题目内容
2.稀硫酸中插一块铜片,加入少量下列物质并充分振荡后,铜可能没有发生反应的是( )| A. | 硫酸铁晶体 | B. | 浓硝酸 | C. | 硝酸锌晶体 | D. | 浓硫酸 |
分析 铜与稀硫酸不反应,加入某种物质后能溶解,说明所加物质在酸性条件下具有强氧化性,可与铜发生氧化还原反应生成可溶性铜盐,以此解答.
解答 解:A、硫酸铁晶体,铜与铁离子发生氧化还原反应生成亚铁离子和铜离子,所以铜发生反应,故A不选;
B、铜与浓硝酸反应生成硝酸铜和二氧化氮气体,所以铜发生反应,故B不选;
C、铜片不溶于非氧化性酸中,但稀硫酸中加入硝酸锌后,溶液中存在H+和NO3-,相当于稀硝酸,铜片能溶于稀硝酸中,发生发生反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,铜发生反应,故C不选;
D、加入浓硫酸,不发生反应,故D选;
故选D.
点评 本题考查铜、硝酸的化学性质,设计新颖,针对性强,注重答题的灵活性,属于中等难度试题的考查.掌握物质的性质是解题的关键,另外还要注意在酸性环境下硝酸根具有强氧化性.

练习册系列答案
相关题目
5.25℃时,水的电离达到平衡:H2O?H++OH-△H>0,下列叙述正确的是( )
| A. | 向水中加入稀氨水,平衡逆向移动,c(OH-)降低 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 | |
| C. | 降温,使平衡左移,c(H+)减小,溶液呈碱性 | |
| D. | 将水加热,Kw增大,pH不变 |
6.下列电离方程式中,正确的是( )
| A. | Fe2(SO4)3═2Fe+3+3SO4-2 | B. | Ba(OH)2═Ba2++2(OH-) | ||
| C. | H2SO4═2H++SO42- | D. | Na2CO3═Na2++CO32- |
10.硫酸的工业制备中,混合气体的组成是:SO2占7%、O2占11%,其余的是N2和CO2,现有100体积混合气体进入接触室反应后,导出的气体恢复到原温度和压强,变为97.2体积,则SO2的转化率约为( )
| A. | 60% | B. | 70% | C. | 80% | D. | 90% |
14.在标准状况时,下列物质的体积约为22.4L的是( )
| A. | 1 mol H2O | B. | 16 g O2 | C. | 1 mol Fe | D. | 2 g H2 |
12.日常生活中我们经常用到一些消毒剂,下列有关说法正确的是( )
| A. | 过氧化氢有“绿色氧化剂”之称,故过氧化氢只能作氧化剂 | |
| B. | 氯气常用于自来水的杀菌消毒,其中起杀菌消毒作用的是氯气 | |
| C. | 过氧乙酸(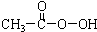 )分子中既有极性键又有非极性键 )分子中既有极性键又有非极性键 | |
| D. | 4.8g臭氧与3.36L氧气含有的原子总数相等 |
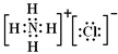 ,氧化钠的电子式
,氧化钠的电子式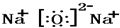 ,CO2的电子式
,CO2的电子式 .
.