题目内容
5.下列说法正确的是( )| A. | 离子化合物中不可能含有共价键 | |
| B. | 由非金属元素组成的化合物不一定是共价化合物 | |
| C. | 非极性键只存在于双原子单质分子里 | |
| D. | 金属元素和非金属元素形成的化合物中一定含有离子键 |
分析 一般来说,活泼金属与活泼非金属元素之间形成的化学键为离子键,相同非金属原子之间形成的共价键为非极性共价键,不同原子之间形成的为极性共价键;
离子化合物中一定含有离子键,可能含有共价键,共价化合物中只含共价键,一定不含离子键;非金属原子间可能形成离子化合物,如铵盐,据此分析.
解答 解:A.离子化合物中一定含有离子键,可能含有共价键,如KOH,故A错误;
B.由非金属元素组成的化合物不一定是共价化合物,也可能形成离子化合物,如铵盐,故B正确;
C.非极性键也可能存在于化合物中,如过氧化氢中含有O-O非极性键,故C错误;
D.金属元素和非金属元素形成的化合物中可能含有共价键,如氯化铝,故D错误;
故选B.
点评 本题考查化合物和化学键的关系,明确共价化合物和离子化合物的概念是解本题关键,注意二者的区别,难度不大.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案
相关题目
16.反应2A(g)?2B(s)+C(g)△H>0,要使逆反应速率降低,应采取的措施是( )
| A. | 减压 | B. | 升温 | ||
| C. | 加压 | D. | 从体系中分离出一部分B物质 |
13.-定条件下,在容积为2L的密闭容器中发生反应:2A(g)+B(g)?2C(g),己知起始投入4molA(g)和2molB(g),经2s后测得C的浓度为0.6mol•L-1,并且2s后各组分浓度不再改变.下列说法正确的是( )
| A. | 2s内用物质A表示的平均反应速率为0.3mol•L-1•s-1 | |
| B. | 2s内用物质B表示的平均反应速率为0.6 mol•L-1•s-1 | |
| C. | 2s后每有0.6 mol的物质B生成,同时就有0.6 mol物质C生成 | |
| D. | 2s时物质B的物质的量浓度为1.4mol•L-1 |
20.下列说法正确的是( )
| A. | 酸雨和温室效应都与化石燃料的使用有关 | |
| B. | 水体富营养化主要是因为水中含有较多的碳、氮等元素 | |
| C. | 天然气水合物,又称可燃冰,其主要可燃成分是氢气 | |
| D. | 聚酯纤维和光导纤维都是有机高分子材料 |
6.某100mL溶液可能含有Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如下:(所加试剂均过量,气体全部逸出)下列说法正确的是( )
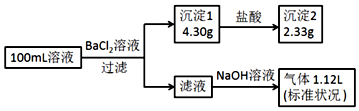

| A. | 原溶液一定存在CO32-和SO42-,一定不存在Fe3+ | |
| B. | 原溶液一定存在Cl-和Na+ | |
| C. | 原溶液中c(Cl-)≥0.2mol•L-1 | |
| D. | 若原溶液中c(NH4+)=0.05mol•L-1 |
3.某气态烃1mol能与2mol HBr完全加成,加成后产物分子上的氢原子又可被4mol Cl2完全取代,则此气态烃可能是( )
| A. | CH≡CH | B. | CH≡C-CH3 | C. | CH2=CH-CH=CH2 | D. | CH2=C(CH3)2 |




 ,C
,C .
. ; 反应⑦:
; 反应⑦: .
.