题目内容
作为应对油气时代过后能源问题的一条解决途径,甲醇受到越来越多的关注。已知在常温常压条件下,1gCH3OH(l)完全燃烧释放出22.7kJ的热量,则表示甲醇燃烧热的热化学方程式为
A.CH3OH(l) +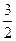 O2(g) ="=" CO2(g) + 2H2O(l);△H=-726.4kJ/mol O2(g) ="=" CO2(g) + 2H2O(l);△H=-726.4kJ/mol |
| B.2CH3OH(l) + 3O2(g) ="=" 2CO2(g) + 4H2O(g);△H=-1452.8kJ/mol |
C.CH3OH(l) +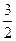 O2(g) ="=" CO2(g) + 2H2O(l);△H=726.4kJ/mol O2(g) ="=" CO2(g) + 2H2O(l);△H=726.4kJ/mol |
| D.2CH3OH(l) + 3O2(g) ="=" 2 CO2(g) + 4H2O(l);△H=-1452.8kJ/mol |
A
略

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目



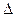 H = —142.9kJ·molˉl
H = —142.9kJ·molˉl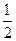 O 2(g) = H2O(1)
O 2(g) = H2O(1)