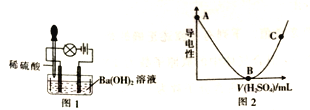
题目内容
【题目】溴化钙是一种重要的化工原料,制备CaBr2·2H2O 的主要流程如下:
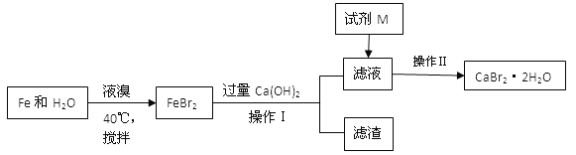
下列说法不正确的是
A. 试剂M 是HBr,加入HBr的目的是除去过量的Ca(OH)2
B. 操作I为过滤,滤渣为Fe、Fe(OH)2和Fe(OH)3;操作Ⅱ为重结晶,具体操作步骤为蒸发浓缩、冷却结晶、洗涤、干燥
C. 制得的CaBr2·2H2O 可以通过以下方法测定纯度:称取一定量的样品溶于水,滴入足量Na2CO3 溶液,充分反应后过滤,将滤渣洗涤、烘干、冷却、称量,计算便得出CaBr2·2H2O的纯度
D. 工业上也可以将氨气通入石灰乳,并加入溴,于65℃进行反应,制得溴化钙,此反应中还会生成一种无色气体,该反应的化学方程式为3Ca(OH)2+3Br2+2NH3 ![]() 3CaBr2+N2+6H2O
3CaBr2+N2+6H2O
【答案】B
【解析】Fe与溴单质反应生成FeBr2 ,加过量的氢氧化钙,生成氢氧化亚铁沉淀,氢氧化亚铁易被氧气氧化为氢氧化铁,过滤得到滤液中主要CaBr2 ,在滤液中加HBr中和多余的氢氧化钙,然后蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到CaBr22H2O晶体。A. 根据上述分析,溴化亚铁溶液中加入过量的氢氧化钙,过滤得到的滤液含有溴化钙和氢氧化钙,加溴化氢除去多余的氢氧化钙,则加入的M为HBr,故A正确;B. 氢氧化亚铁易被氧气氧化为氢氧化铁,操作I为过滤,滤渣为Fe和Fe(OH)3,故B错误; C.称取一定量的样品溶于水,滴入足量Na2CO3 溶液,充分反应后过滤得到生成的碳酸钙沉淀,将滤渣洗涤、烘干、冷却、称量氧化钙的质量,可以得出CaBr2·2H2O的纯度,故C正确;D. 3Ca(OH)2+3Br2+2NH3 ![]() 3CaBr2+N2+6H2O,因此工业上也可以将氨气通入石灰乳,并加入溴,于65℃进行反应,制得溴化钙,故D正确;故选B。
3CaBr2+N2+6H2O,因此工业上也可以将氨气通入石灰乳,并加入溴,于65℃进行反应,制得溴化钙,故D正确;故选B。

 发散思维新课堂系列答案
发散思维新课堂系列答案【题目】镁合金及镁的化合物在生产、生活中有着广泛的应用。
(1)镁在元素周期表中的位置是____________。
(2)用水氯镁石(主要成分为MgCl2·6H2O)制备金属镁的关键流程如下:
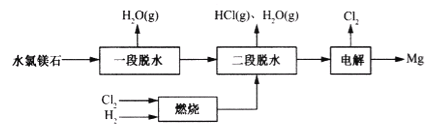
① 一段脱水后,残留固体质量占原样品质量的64.5%,试确定生成物的化学式__________。② 二段脱水时,溶入H2和Cl2燃烧产物的目的是__________。
③ 该工艺中可循环使用的物质有_____________
(3)储氢材料Mg(AlH4)2在110-200℃的反应为:Mg(AlH4)2 =MgH2 +2Al+3H2↑,每转移6mol电子生成氢气的物质的量为__________mol。
(4)碱式碳酸镁密度小,是橡胶制品的优良填料,可用复盐MgCO3·(NH4)2CO3·2H2O作原料制备。
① 40℃时,复盐开始热解生成MgCO3·3H2O,并有气体产生,该反应的化学方程式为________。
② 制备过程中,需要用到卤水(氯化镁溶液)。某科研小组用沉淀滴定法分析产品中Cl-的含量,称取6.1000g产品用适量硝酸溶解,经稀释等步骤最终配得500mL 的溶液。
a.准确量取25.00mL 待测液,用0.1000 mol/ L AgNO3 标准液滴定,滴定前后滴定管中的液面读数如图所示,则滴定过程中消耗标准液的体积为______________mL。
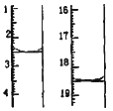
b.
AgCl | AgBr | AgI | Ag2CrO4 | |
Ksp | 2×10-10 | 5.4×10-13 | 8.3×10-17 | 2×10-12 |
颜色 | 白 | 淡黄 | 黄 | 砖红 |
参照上表数据及信息分析,滴定时可以作指示剂的是________(填数字序号)。
① CaCl2 ② NaBr ③ NaI ④ K2CrO4
c.滴定时,应将溶液调成中性,不能是强酸性或强碱性,其中不能是强碱性的原因是________。
d.产品中氯的质量分数为___________(保留三位有效数字)。