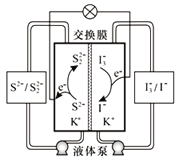
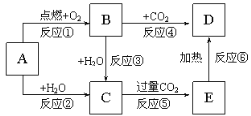
��Ŀ����
����Ŀ��ijһԪ���ᣨ��HA��ʾ����ˮ�еĵ��뷽��ʽ��HA![]() H����A�����ش��������⣺
H����A�����ش��������⣺
�� ��ˮ�м�������HA��ˮ�ĵ���ƽ�⽫��________����������������������Ӧ�����ƶ���������_______��
�� �����������Һ�м�������NaCl��Һ������ƽ�⽫��________����������������������Ӧ�����ƶ�����Һ��c(A��)��____________������������������С������������������Һ��c(OH��)��____________������������������С����������������
�� ��25 ���£���a mol��L��1�İ�ˮ��0.01 mol��L��1������������ϣ���Ӧƽ��ʱ��Һ��c(NH![]() )=c(Cl��)������Һ��________�ԣ�����������������������������a_____0.01����������������С�������������������ú�a�Ĵ���ʽ��ʾNH3��H2O�ĵ��볣��Kb��_________________��
)=c(Cl��)������Һ��________�ԣ�����������������������������a_____0.01����������������С�������������������ú�a�Ĵ���ʽ��ʾNH3��H2O�ĵ��볣��Kb��_________________��
���𰸡��� c(H��)����ƽ�����Сc(H��)�ķ����淴Ӧ�����ƶ� �� ��С ���� �� ���� 10��9/(a��0.01)mol��L��1
��������
��1��HAΪһԪ���ᣬ����ˮ�м���HA����ˮ�ĵ���ƽ�����������ã������淴Ӧ�����ƶ���ˮ�д���H2O![]() H����OH����HAΪһԪ���ᣬ��������ˮ��HA�����H������Һc(H��)����ʹˮ�ĵ���ƽ�����淴Ӧ������У�
H����OH����HAΪһԪ���ᣬ��������ˮ��HA�����H������Һc(H��)����ʹˮ�ĵ���ƽ�����淴Ӧ������У�
��2����(1)��Һ�м���NaCl��Һ��NaCl�����뷴Ӧ��������NaCl��Һϡ��(1)������Һ����ʹHA�������룬HA�ĵ���ƽ��������Ӧ�����ƶ�����Ȼ����ƽ��������Ӧ�����ƶ�������Һ�����Ҳ�������c(A��)��С��c(H��)��С������ˮ�����ӻ���c(OH��)����
��3��������Һ���ֵ����ԣ������c(NH4��)��c(H��)=c(OH��)��c(Cl��)����Ϊc(NH4��)=c(Cl��)�����c(H��)=c(OH��)����Һ�����ԣ���a=0.01mol��L��1ʱ��������Һ�������ϣ�ǡ����ȫ����NH4Cl����Һ�����ԣ���Һ�����ԣ����NH3��H2O����������a>0.01mol��L��1�����볣��ֻ���¶ȵ�Ӱ�죬��Һ��c(OH��)=10��7mol��L��1��c(NH4��)=c(Cl��)=0.01mol��L��1/2=5��10��3mol��L��1�����������غ㣬c(NH3��H2O)=(a/2mol��L��1��5��10��3mol��L��1)��NH3��H2O����ƽ�ⳣ��Kb=c(NH4��)��c(OH��)/c(NH3��H2O)��������ֵ���ó�NH3��H2O�ĵ���ƽ�ⳣ��Kb=10��9/(a��0.01)��

����Ŀ����֪A(g)+B(g)![]() C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
�¶�/�� | 700 | 800 | 830 | 1000 | 1200 |
ƽ�ⳣ�� | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
830��ʱ����һ��2 L���ܱ������г���0.2 mol��A��0.8 mol��B����Ӧ��ʼ4 s��A��ƽ����Ӧ������(A)=0.005 mol��(L��s)������˵����ȷ����
A. 4 sʱc(B)Ϊ0.38 mol��L
B. 830���ƽ��ʱ��A��ת����Ϊ20��
C. ��Ӧ��ƽ��������¶ȣ�ƽ�������ƶ�
D. 1200��ʱ��ӦC(g)+D(g)![]() A(g)+B(g)��ƽ�ⳣ��Ϊ0.4
A(g)+B(g)��ƽ�ⳣ��Ϊ0.4