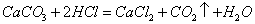��Ŀ����
��14�֣���ͭ��( CuFeS2)����ȡͭ���仯�������Ҫԭ��֮һ���������Ʊ������Ļ����
��1������ұ��ͭ�ķ�ӦΪ��8 CuFeS2+21O2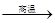 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
CuFeS2��Fe�Ļ��ϼ�Ϊ+2����Ӧ�б�������Ԫ����___________����Ԫ�ط��ţ���
��2��������ұ�������в�������SO2�����д���������������___________������ţ���
a���߿��ŷ� b�������Ʊ�����
c����Ũ�������� d���ô�����Һ������Na2SO3
��3�������û�������������ͭ���м���̻ᷢ��Cu2O��Cu2S�ڸ�����ת��ΪCu���ų�SO2����ķ�Ӧ����Cu2O��Cu2S������ȫ��Ӧ��Cu2O��Cu2S�����ʵ���֮��Ϊ_____��Cu2S��HNO3�����·�Ӧ��3Cu2S+22HNO3=6Cu(NO3)2+3H2SO4+10NO +8H2O������11.2LNO(��״��)����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ__________��
+8H2O������11.2LNO(��״��)����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ__________��
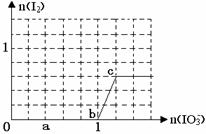
��4�������������(K2S2O8)����ǿ�����ԣ��ɽ�I������ΪI2��S2O82��+2I��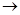 2SO42��+I2ͨ���ı䷴Ӧ;����Fe3+��Fe2+���ɴ�������Ӧ���������ӷ���ʽ��ʾFe2+��������Ӧ�Ĵ����̣�____________________________��______________________________��
2SO42��+I2ͨ���ı䷴Ӧ;����Fe3+��Fe2+���ɴ�������Ӧ���������ӷ���ʽ��ʾFe2+��������Ӧ�Ĵ����̣�____________________________��______________________________��
��1������ұ��ͭ�ķ�ӦΪ��8 CuFeS2+21O2
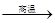 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2CuFeS2��Fe�Ļ��ϼ�Ϊ+2����Ӧ�б�������Ԫ����___________����Ԫ�ط��ţ���
��2��������ұ�������в�������SO2�����д���������������___________������ţ���
a���߿��ŷ� b�������Ʊ�����
c����Ũ�������� d���ô�����Һ������Na2SO3
��3�������û�������������ͭ���м���̻ᷢ��Cu2O��Cu2S�ڸ�����ת��ΪCu���ų�SO2����ķ�Ӧ����Cu2O��Cu2S������ȫ��Ӧ��Cu2O��Cu2S�����ʵ���֮��Ϊ_____��Cu2S��HNO3�����·�Ӧ��3Cu2S+22HNO3=6Cu(NO3)2+3H2SO4+10NO
 +8H2O������11.2LNO(��״��)����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ__________��
+8H2O������11.2LNO(��״��)����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ__________����4�������������(K2S2O8)����ǿ�����ԣ��ɽ�I������ΪI2��S2O82��+2I��
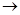 2SO42��+I2ͨ���ı䷴Ӧ;����Fe3+��Fe2+���ɴ�������Ӧ���������ӷ���ʽ��ʾFe2+��������Ӧ�Ĵ����̣�____________________________��______________________________��
2SO42��+I2ͨ���ı䷴Ӧ;����Fe3+��Fe2+���ɴ�������Ӧ���������ӷ���ʽ��ʾFe2+��������Ӧ�Ĵ����̣�____________________________��______________________________��(1)Fe��S (2)bd (3)2:1��1.5mol
(4)S2O82��+2Fe2+=2SO42��+2Fe3+ 2Fe3++2I��=2Fe2++I2
(4)S2O82��+2Fe2+=2SO42��+2Fe3+ 2Fe3++2I��=2Fe2++I2
��
�����������1��CuFeS2��Fe�� Cu��S���ϼ�Ϊ+2��+2����2�����ϼ����ߵ�Ԫ����Fe��S�����ϼ۽��͵�Ԫ����Cu��O��
��2������������Ⱦ���������ܸ߿��ŷţ����������Ũ�����Ӧ��������Ũ�������գ��ɰѶ������������Ϊ������������98.3%Ũ���������Ƶ����ᣬ������Na2CO3��Һ����SO2��Na2SO3��
��3��Cu2O��Cu2S��Ӧ����ʽΪ2Cu2O+Cu2S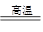 6Cu+SO2��3Cu2S+22HNO3=6Cu(NO3)2+3H2SO4+10NO��+8H2O��Ӧ��ת�Ƶ�����Ϊ30����������0.5molNOʱת�Ƶ�����Ϊ1.5mol��
6Cu+SO2��3Cu2S+22HNO3=6Cu(NO3)2+3H2SO4+10NO��+8H2O��Ӧ��ת�Ƶ�����Ϊ30����������0.5molNOʱת�Ƶ�����Ϊ1.5mol��
��4�������μӻ�ѧ��ӦȻ������������Fe2+��������Ӧ�����̿ɱ�ʾΪS2O82��+2Fe2+=2SO42��+2Fe3+��2Fe3++2I��=2Fe2++I2������ʾFe3+��������Ӧ�Ĵ����̿ɱ�ʾΪ2Fe3++2I��=2Fe2++I2��S2O82��+2Fe2+=2SO42��+2Fe3+��
�����������μӻ�ѧ��Ӧ����������������
�����������1��CuFeS2��Fe�� Cu��S���ϼ�Ϊ+2��+2����2�����ϼ����ߵ�Ԫ����Fe��S�����ϼ۽��͵�Ԫ����Cu��O��
��2������������Ⱦ���������ܸ߿��ŷţ����������Ũ�����Ӧ��������Ũ�������գ��ɰѶ������������Ϊ������������98.3%Ũ���������Ƶ����ᣬ������Na2CO3��Һ����SO2��Na2SO3��
��3��Cu2O��Cu2S��Ӧ����ʽΪ2Cu2O+Cu2S
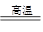 6Cu+SO2��3Cu2S+22HNO3=6Cu(NO3)2+3H2SO4+10NO��+8H2O��Ӧ��ת�Ƶ�����Ϊ30����������0.5molNOʱת�Ƶ�����Ϊ1.5mol��
6Cu+SO2��3Cu2S+22HNO3=6Cu(NO3)2+3H2SO4+10NO��+8H2O��Ӧ��ת�Ƶ�����Ϊ30����������0.5molNOʱת�Ƶ�����Ϊ1.5mol����4�������μӻ�ѧ��ӦȻ������������Fe2+��������Ӧ�����̿ɱ�ʾΪS2O82��+2Fe2+=2SO42��+2Fe3+��2Fe3++2I��=2Fe2++I2������ʾFe3+��������Ӧ�Ĵ����̿ɱ�ʾΪ2Fe3++2I��=2Fe2++I2��S2O82��+2Fe2+=2SO42��+2Fe3+��
�����������μӻ�ѧ��Ӧ����������������

��ϰ��ϵ�д�
 ����С��ʿ���������ϵ�д�
����С��ʿ���������ϵ�д�
�����Ŀ