题目内容
(8分)稀HNO3和锌反应的化学方程式如下:
4Zn + 10 HNO3= 4Zn(NO3)2 +N2O↑+5H2O
(1)请标明上述化学方程式中电子转移的方向和数目。
(2)该反应中还原剂是 ,还原产物是 ,每2 mol Zn参加反应,转移的电子 个。
(3)上述反应中,HNO3没有全部参加氧化还原反应,没有参加氧化还原反应的硝酸与总硝酸的物质的量之比是 。
4Zn + 10 HNO3= 4Zn(NO3)2 +N2O↑+5H2O
(1)请标明上述化学方程式中电子转移的方向和数目。
(2)该反应中还原剂是 ,还原产物是 ,每2 mol Zn参加反应,转移的电子 个。
(3)上述反应中,HNO3没有全部参加氧化还原反应,没有参加氧化还原反应的硝酸与总硝酸的物质的量之比是 。
(8分)(1) 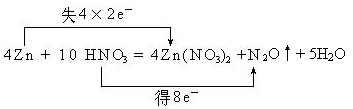 (2分)
(2分)
(2)Zn (1分) N2O(1分) 4NA(2分) (3)4:5(2分)
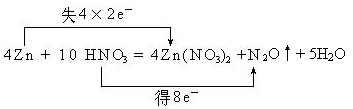 (2分)
(2分)(2)Zn (1分) N2O(1分) 4NA(2分) (3)4:5(2分)
考查氧化还原反应的有关判断和计算。
(1)根据反应的方程式可知,锌元素的化合价从0价升高到+2价,失去2个电子,作还原剂,而硝酸锌是氧化产物;硝酸中氮元素的化合价从+5价降低到+1价,得到4个电子,所以硝酸是氧化剂,N2O是还原产物,因此根据电子的得失守恒可知,表示为
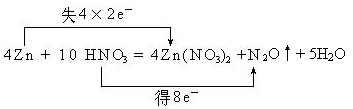 。
。
(2)根据反应的方程式可知,2 mol Zn参加反应,转移的电子的物质的量是4mol,个数是4NA个。
(3)根据方程式可知,没有参加氧化还原反应的硝酸与总硝酸的物质的量之比是4︰5。
(1)根据反应的方程式可知,锌元素的化合价从0价升高到+2价,失去2个电子,作还原剂,而硝酸锌是氧化产物;硝酸中氮元素的化合价从+5价降低到+1价,得到4个电子,所以硝酸是氧化剂,N2O是还原产物,因此根据电子的得失守恒可知,表示为
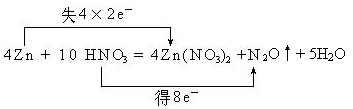 。
。(2)根据反应的方程式可知,2 mol Zn参加反应,转移的电子的物质的量是4mol,个数是4NA个。
(3)根据方程式可知,没有参加氧化还原反应的硝酸与总硝酸的物质的量之比是4︰5。

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案
相关题目
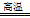 Fe+TiO2+H2O,下列有关该反应的说法错误的是( )
Fe+TiO2+H2O,下列有关该反应的说法错误的是( )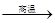 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2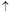 +8H2O若生成11.2LNO(标准状况),则反应中转移电子的物质的量为__________。
+8H2O若生成11.2LNO(标准状况),则反应中转移电子的物质的量为__________。 2SO42-+I2通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe2+对上述反应的催化过程:____________________________、______________________________。
2SO42-+I2通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe2+对上述反应的催化过程:____________________________、______________________________。