题目内容
【题目】(1)反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)在一容积可变的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g)在一容积可变的密闭容器中进行,试回答:
①增加Fe的量,其反应速率____(填“增大”、“不变”或“减小”,下同)。
②将容器的体积缩小一半,其反应速率____。
③保持体积不变,充入He,其反应速率____。
④保持压强不变,充入He,其反应速率_____。
(2)氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和NH3,在一定条件下发生反应:6NO(g)+4NH3(g)![]() 5N2(g)+6H2O(g)。
5N2(g)+6H2O(g)。
①能说明该反应已达到平衡状态的标志是____(填字母序号)
a.反应速率5v(NH3)=4v(N2)
b.单位时间里每生成5mol N2,同时生成4mol NH3
c.容器内N2的物质的量分数不再随时间而发生变化
d.容器内n(NO):n(NH3):n(N2):n(H2O)=6:4:5:6
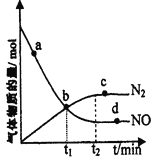
②某次实验中测得容器内NO及N2的物质的量随时间变化如图所示,图中v(正)与v(逆)相等的点为_____(选填字母)。
(3)298K时,若已知生成标准状况下2.24LNH3时放出热量为4.62kJ。写出合成氨反应的热化学方程式____。
(4)一定条件下,在2L密闭容器内,反应2NO2(g)=N2O4(g)△H=-180kJ·mol-1,n(NO2)随时间变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO2)/mol | 0.040 | 0.020 | 0.010 | 0.005 | 0.005 | 0.005 |
用NO2表示0~2s内该反应的平均速度____。在第5s时,NO2的转化率为____。根据上表可以看出,随着反应进行,反应速率逐渐减小,其原因是____。
【答案】不变 增大 不变 减小 bc cd N2(g)+3H2(g)=2NH3(g)△H=-92.4kJ/mol 0.0075mol·L-1·s-1 87.5% 随着反应的进行,二氧化氮的物质的量浓度减小
【解析】
(1)①Fe为固体,浓度视为常数,即增加Fe的量,化学反应速率不变;
②容器的体积缩小一半,即组分浓度增大,化学反应速率增大;
③He属于非反应气体,恒容状态下,充入He,组分的浓度保持不变,化学反应速率保持不变;
④恒压下,充入He,容器的体积增大,组分的浓度降低,化学反应速率减小;
(2)①a、没有指明反应进行的方向,即无法判断是否达到平衡,故a不符合题意;
b、生成N2反应向正反应方向进行,生成NH3反应向逆反应方向进行,且生成量之比等于系数之比,即能说明反应达到平衡,故b符合题意;
c、根据化学平衡状态的定义,N2的物质的量分数不再随时间发生变化,能说明反应达到平衡,故c符合题意;
d、题中没有说明通入NO和NH3的量,无法判断是否达到平衡,故d不符合题意;
答案选bc;
②v(正)与v(逆)相等的点,说明反应达到平衡,根据图象,达到平衡的点是cd;
(3)生成标准状况下2.24L的NH3,即生成0.1mol的NH3,得出生成2molNH3,放出的热量为92.4kJ,合成氨的热化学方程式为N2(g)+3H2(g)=2NH3(g)△H=-92.4kJ/mol;
(4)根据化学反应速率的数学表达式,v(NO2)=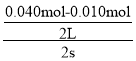 =0.0075mol/(L·s);5s内消耗NO2的物质的量为(0.040mol-0.005mol)=0.035mol,即NO2的转化率为
=0.0075mol/(L·s);5s内消耗NO2的物质的量为(0.040mol-0.005mol)=0.035mol,即NO2的转化率为![]() ×100%=87.5%;随着反应的进行,NO2的物质的量浓度减小,物质的量浓度起主导作用,即化学反应速率减小。
×100%=87.5%;随着反应的进行,NO2的物质的量浓度减小,物质的量浓度起主导作用,即化学反应速率减小。

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案