题目内容
12.下列与含氯化合物有关的说法正确的是( )| A. | HClO是弱酸,所以NaClO是弱电解质 | |
| B. | 电解NaCl 溶液得到22.4L H2,理论上需要转移2NA个电子(NA阿伏伽德罗常数) | |
| C. | HCl 溶液和NaCl溶液均通过离子导电,所以HCl 和NaCl均是离子化合物 | |
| D. | 向沸水中逐滴加入少量饱和FeCl3 溶液,可制得Fe(OH)3胶体 |
分析 A.NaClO为盐,在水溶液完全电离;
B.状况未知,不能利用体积计算转移电子数;
C.溶液导电与离子有关,不能判断物质中化学键;
D.氯化铁水解可制备胶体.
解答 解:A.HClO是弱酸,而NaClO是强电解质,故A错误;
B.电解NaCl 溶液得到22.4L H2,状况未知,不能利用体积计算转移电子数,故B错误;
C.HCl 溶液和NaCl溶液均通过离子导电,与电离产生自由移动的离子有关,但HCl只含共价键为共价化合物,NaCl含离子键为离子化合物,故C错误;
D.沸水中逐滴加入少量饱和FeCl3 溶液,发生水解反应可制得Fe(OH)3胶体,故D正确;
故选D.
点评 本题考查物质的性质,为高频考点,综合考查元素化合物知识及反应原理等,涉及电解质、化学键与物质类别、电解、水解等,注重高频考点的考查,题目难度不大.

练习册系列答案
相关题目
4.下列关于有机物莽草酸(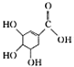 )和鞣酸(
)和鞣酸(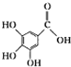 )的叙述中,正确的是( )
)的叙述中,正确的是( )
 )和鞣酸(
)和鞣酸( )的叙述中,正确的是( )
)的叙述中,正确的是( )| A. | 两种有机物中含有完全相同的官能团 | |
| B. | 两种酸都能与溴水反应,且反应类型相同 | |
| C. | 分别向两种酸中滴加三氯化铁溶液,均发生显色反应 | |
| D. | 等物质的量的两种酸与NaOH反应,消耗NaOH的量不同 |
3.下列微粒之间能形成离子键的是( )
①K+
②质量数为19,中子数为10的原子
③第三周期半径最大的原子(Ar除外)
④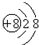
①K+
②质量数为19,中子数为10的原子
③第三周期半径最大的原子(Ar除外)
④
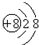
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
20.下列图示实验正确的是( )
| A. | 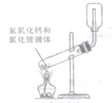 实验室制备氨气 | B. | 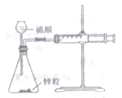 测量锌和硫酸反应的速率 | ||
| C. |  铁的吸氧腐蚀 | D. | 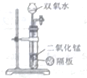 实验室制氧气 |
7.下列有关有机反应的叙述正确的是( )
| A. | 采用分子筛固体酸作为苯和丙烯反应的催化剂来制备异丙苯,符合绿色化学工艺 | |
| B. | 一定条件下,所有的醇均能发生脱水反应形成碳碳双键或碳碳三键 | |
| C. | 石油的裂化、裂解都是化学变化,煤的气化、液化都是物理变化 | |
| D. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
17.下列反应中,属于消去反应的是( )
| A. | CH3CH=CH2+Br2$\stackrel{CCI_{4}}{→}$CH3CHBrCH2Br | |
| B. | CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$CH2=CH2+H2O | |
| C. | CH3CH2OH+Na→CH3CH2ONa+H2↑ | |
| D. | C6H6+HNO3$→_{△}^{浓H_{2}SO_{4}}$C6H5NO2+H2O |
4.甲、乙两种有机物的最简式均为CH2O.下列叙述一定正确的是( )
| A. | 甲乙互为同系物 | |
| B. | 甲乙互为同分异构体 | |
| C. | 等物质的量的甲、乙完全燃烧所耗O2的物质的量相等 | |
| D. | 甲、乙分别充分燃烧,产生CO2和H2O的物质的量之比均为1:1 |
 Ⅰ.甲硅烷(SiH4)常温下是一种无色气体,遇空气发生自燃.
Ⅰ.甲硅烷(SiH4)常温下是一种无色气体,遇空气发生自燃.