题目内容
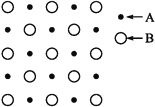
【题目】我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表),经X射线衍射测得R的局部结构如图所示,下列说法正确的是( )
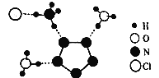
A.R中两种阳离子的中心原子的杂化轨道类型相同,但化学键类型不同
B.1molR中σ键总数为15个
C.N5-中参与形成的大π键电子数为6个
D.已知图中虚线代表氢键,其中一个表示为(NH4)N﹣H···Cl,则化合物R中共有4个不同类型氢键
【答案】C
【解析】
A.R中阳离子为NH4+中心原子为sp3杂化轨道,形成3个σ键和1个配位键,另一种阳离子为H3O+,中心原子为sp3杂化轨道,形成2个σ键和1个配位键键,所以二者中心原子的杂化轨道类型相同,化学键类型相同,故A错误;
B.据图可知1molR中σ键总数为15NA,故B错误;
C.N5-中每个N形成两条共价键,pz轨道留有一个单电子,5个N的5个pz轨道交盖形成离域大π键;N5-的价电子总数为5×5+1=26,σ键个数为5,每个氮原子有1对孤电子对,且未参与形成大π键,所以参与形成大π键的电子数为26-5×2-5×2=6,故C正确;
D.据图可知除(NH4+)N-H···Cl外还有(H3O+)O-H···N(N5-)、(NH4+)N-H···N(N5-)两种氢键,共三种,故D错误;
故答案为C。

练习册系列答案
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目