题目内容
【题目】工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示:
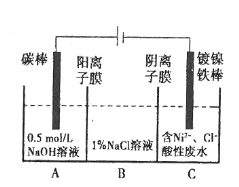
已知:①Ni2+在弱酸性溶液中发生水解②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)。下列说法不正确的是
A.碳棒上发生的电极反应:4OH-—4e-=O2↑+2H2O
B.为了提高Ni的产率,电解过程中需要控制废水pH
C.电解过程中,B中NaCl溶液的物质的量浓度将不断减少
D.若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
【答案】C
【解析】
A.由图知,碳棒与电源正极相连是电解池的阳极,电极反应4OH--4e-=2H2O+O2↑,故A正确;
B.因Ni2+在弱酸性溶液中易发生水解;氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度),为了提高Ni的产率,电解过程中需要控制废水pH,故B正确;
C.镀镍铁棒与电源负极相连是电解池的阴极,电极反应Ni2++2e-=Ni.电解过程中为平衡A、C中的电荷,A中的Na+和C中的Cl-分别通过阳离子膜和阴离子膜移向B中,这使B中NaCl溶液的物质的量浓度不断增大,故C错误;
D.若将图中阳离子膜去掉,由于放电顺序Cl->OH-,则Cl-移向阳极放电:2Cl --2e-=Cl2↑,电解反应总方程式会发生改变,故D正确;
故选:C。

 阅读快车系列答案
阅读快车系列答案【题目】在2L密闭容器内,800℃时,加入一定量的NO、O2,发生如下反应:2NO(g)+O2(g) ![]() 2NO2(g) ΔH< 0,反应过程中n(NO)随时间的变化如下表:
2NO2(g) ΔH< 0,反应过程中n(NO)随时间的变化如下表:
时间/s | 0 | 10 | 20 | 30 | 40 | 50 |
n(NO)/mol | 0. 20 | 0. 10 | 0.08 | 0.07 | 0.07 | 0.07 |
(1)计算该反应在20秒内用O2表示的反应速率v(O2)= ______________ ;
(2)写出该反应的平衡常数表达式____________。升高温度该反应平衡常数会_______(填“增大”“减小”或“不变”)
(3)下列示意图正确且能说明反应达到平衡状态的是___________

(4)能使该反应的反应速率增大,且NO的平衡转化率也增大的是__________。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
(5)已知:2NO(g)![]() N2(g)+O2(g) K1=1×1030;2CO2(g)
N2(g)+O2(g) K1=1×1030;2CO2(g)![]() 2CO(g)+O2(g)K2= 4×10-92。随着轿车进入家庭,汽车尾气(含碳氢化合物、一氧化碳、二氧化硫、一氧化氮等物质)污染成为备受关注的环境问题,某市政府要求全市新有汽车尾气处理装置完成改装,改装后的尾气处理装置主要是加了有效催化剂。请你根据以上有关数据回答:
2CO(g)+O2(g)K2= 4×10-92。随着轿车进入家庭,汽车尾气(含碳氢化合物、一氧化碳、二氧化硫、一氧化氮等物质)污染成为备受关注的环境问题,某市政府要求全市新有汽车尾气处理装置完成改装,改装后的尾气处理装置主要是加了有效催化剂。请你根据以上有关数据回答:
①2NO(g)+2CO(g) ![]() N2(g)+ 2CO2(g) K=_____________
N2(g)+ 2CO2(g) K=_____________
②仅使用催化剂_______(填“能”或“否”)消除NO、CO污染气体。