题目内容
14.如图所涉及的物质均为中学化学中的常见物质,它们存在如下转化关系.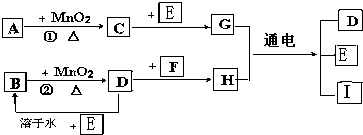
其中
(1)C、D、E、F都为单质,其余为化合物
(2)C、D、E 在常温下为气体,其它物质为固体或液体
(3)A、I 两种化合物的焰色反应分别为紫色和黄色
(4)反应 ①②的一些生成物已经略去,有些反应的条件未列出
(1)写出有关物质的化学式:
AKClO3,DCl2,FNa,INaOH.
(2)指出MnO2在相关反应中的作用:反应 ①中是催化剂,反应 ②中是氧化剂.
(3)写出B与MnO2共热获得D的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2 H2O.
(4)写出G、H混合液通电后发生反应的化学方程式2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑.
分析 A、I 两种化合物的焰色反应分别为紫色和黄色,分别含有K元素、Na元素,A在二氧化锰、加热条件下反应得到气体单质C,应是实验室制备氧气反应,则A为KClO3,C为O2,B与二氧化锰反应得到气体单质D,应是实验室制备氯气,则B为HCl、D为Cl2,D与气体单质E反应后溶于水水得到B,故E为H2,则E与C反应生成G为H2O,氯气与固体单质F反应生成H,电解H水溶液得到氯气、氢气与I,则F为Na、H为NaCl、I为NaOH,据此解答.
解答 解:A、I 两种化合物的焰色反应分别为紫色和黄色,分别含有K元素、Na元素,A在二氧化锰、加热条件下反应得到气体单质C,应是实验室制备氧气反应,则A为KClO3,C为O2,B与二氧化锰反应得到气体单质D,应是实验室制备氯气,则B为HCl、D为Cl2,D与气体单质E反应后溶于水水得到B,故E为H2,则E与C反应生成G为H2O,氯气与固体单质F反应生成H,电解H水溶液得到氯气、氢气与I,则F为Na、H为NaCl、I为NaOH.
(1)由上述分析可知,A为KClO3,D为Cl2,F为Na,I为:NaOH,故答案为:KClO3;Cl2;Na;NaOH;
(2)反应 ①中MnO2是催化剂,反应 ②中MnO2是氧化剂,故答案为:催化;氧化;
(3)B与MnO2共热获得D的离子方程式为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2 H2O;
(4)G、H混合液通电后发生反应的化学方程式:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑,故答案为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑.
点评 本题考查无机物推断,注意根据中学常见二氧化锰参与的反应进行推断,需要学生熟练掌握元素化合物知识,难度中等.

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案| A. | 漂白粉是纯净物,漂白液是混合物 | |
| B. | 漂白粉的有效成分是Ca(ClO)2、CaCl2 | |
| C. | 工业上将氯气通入澄清石灰水制取漂白粉 | |
| D. | 漂白粉使用时要让衣物浸泡一段时间是为了让漂白粉与气中的二氧化碳充分反应生成次氯酸 |
| A. | 1.0mol/L的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| B. | 与铝反应产生大量氢气的溶液:Na+、K+、HCO3-、NO3- | |
| C. | pH=12的溶液:K+、Na+、CH3COO-、Br- | |
| D. | 由水电离产生的c(H+)=10-13mol/L的溶液:NH4+、Ba2+、AlO2-、Cl- |
 有专家指出,如果燃烧产物如CO2、H2O、N2等利用太阳能使它们重新组合能够实现,那么,这不仅可以消除对大气的污染,还可以节约燃料,缓解能源危机.在此构想的物质循环中太阳能最终转化为( )
有专家指出,如果燃烧产物如CO2、H2O、N2等利用太阳能使它们重新组合能够实现,那么,这不仅可以消除对大气的污染,还可以节约燃料,缓解能源危机.在此构想的物质循环中太阳能最终转化为( )| A. | 化学能 | B. | 热能 | C. | 生物能 | D. | 电能 |
| A. | 0.4 mol•L-1 | B. | 0.3 mol•L-1 | C. | 0.2 mol•L-1 | D. | 0.1 mol•L-1 |
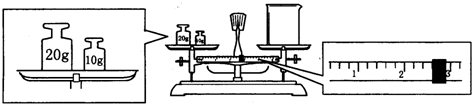
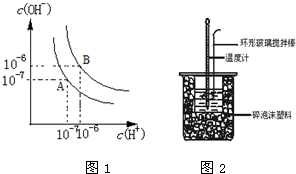 溶液的酸碱性对生产生活都有重要的影响.
溶液的酸碱性对生产生活都有重要的影响.