题目内容
除去下列物质中所含的杂质(括号内为杂质),将选用的试剂和分离方法填在题后的横线上,并写出有关反应的化学方程式,如果是离子反应的写出离子方程式.
(1)Fe2O3(Fe(OH)3) , ;
(2)FeCl3(FeCl2) , ;
(3)FeCl2(CuCl2) , ;
(4)Fe(Al) , .
(1)Fe2O3(Fe(OH)3)
(2)FeCl3(FeCl2)
(3)FeCl2(CuCl2)
(4)Fe(Al)
考点:物质的分离、提纯的基本方法选择与应用,离子方程式的书写,常见金属元素的单质及其化合物的综合应用,物质的分离、提纯和除杂
专题:几种重要的金属及其化合物
分析:(1)Fe(OH)3加热分解生成氧化铁;
(2)氯气与FeCl2反应生成氯化铁;
(3)Fe与CuCl2反应生成氯化亚铁;
(4)Al与NaOH溶液反应,而Fe不能.
(2)氯气与FeCl2反应生成氯化铁;
(3)Fe与CuCl2反应生成氯化亚铁;
(4)Al与NaOH溶液反应,而Fe不能.
解答:
解:(1)Fe(OH)3加热分解生成氧化铁,则选择方法为加热,发生的反应为2Fe(OH)3
Fe2O3+3H2O,故答案为:加热;2Fe(OH)3
Fe2O3+3H2O;
(2)氯气与FeCl2反应生成氯化铁,则选择试剂为通入足量的Cl2,发生的离子反应为2Fe2++Cl2═2Fe3++2Cl-,
故答案为:通入足量的Cl2;2Fe2++Cl2═2Fe3++2Cl-;
(3)Fe与CuCl2反应生成氯化亚铁,则选择的试剂及方法为加入足量铁粉,过滤;发生的离子反应为Fe+Cu2+═Fe2++Cu,
故答案为:加入足量铁粉,过滤;Fe+Cu2+═Fe2++Cu;
(4)Al与NaOH溶液反应,而Fe不能则选择试剂和方法为加入过量的NaOH溶液,过滤,发生的离子反应为2Al+2OH-+2H2O═2AlO2-+3H2↑,
故答案为:加入过量的NaOH溶液,过滤;2Al+2OH-+2H2O═2AlO2-+3H2↑.
| ||
| ||
(2)氯气与FeCl2反应生成氯化铁,则选择试剂为通入足量的Cl2,发生的离子反应为2Fe2++Cl2═2Fe3++2Cl-,
故答案为:通入足量的Cl2;2Fe2++Cl2═2Fe3++2Cl-;
(3)Fe与CuCl2反应生成氯化亚铁,则选择的试剂及方法为加入足量铁粉,过滤;发生的离子反应为Fe+Cu2+═Fe2++Cu,
故答案为:加入足量铁粉,过滤;Fe+Cu2+═Fe2++Cu;
(4)Al与NaOH溶液反应,而Fe不能则选择试剂和方法为加入过量的NaOH溶液,过滤,发生的离子反应为2Al+2OH-+2H2O═2AlO2-+3H2↑,
故答案为:加入过量的NaOH溶液,过滤;2Al+2OH-+2H2O═2AlO2-+3H2↑.
点评:本题考查物质分离提纯方法和选择及金属及化合物的性质,为高频考点,把握物质的性质及性质差异为解答的关键,注意除杂不能引入新杂质,题目难度不大.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
下列说法中,正确的是( )
| A、相邻的原子之间的相互作用叫做化学键 |
| B、金属和非金属元素的相互化合,都能形成离子键 |
| C、非金属元素的原子半径比其离子半径小(氢除外),金属元素的原子的原子半径比其离子半径大 |
| D、甲元素原子半径比乙元素原子半径大,则甲的离子半径一定比乙的原子半径大 |
下列各组物质的主要成分,皆为同一种酸所对应的盐是( )
| A、大理石、重晶石、光卤石 |
| B、小苏打、苏打、大苏打 |
| C、绿矾、胆矾、明矾 |
| D、铝土矿、硫铁矿、磁铁矿 |
航天飞船可用肼(N2H4)作动力源.已知1g液态肼和足量的液态过氧化氢反应生成N2和水蒸气时放出20.05kJ热量,化学方程式如下:N2H4+2H2O2═N2↑+4H2O.下列说法中错误的是( )
| A、该反应中肼作还原剂 |
| B、此情况下,液态肼燃烧生成1molN2时放出的热量为641.6kJ |
| C、肼(N2H4)分子中只存在极性共价键 |
| D、该反应的反应物总能量高于生成物的总能量 |
为了探究锌与稀硫酸的反应速率[以v(H2)表示],向反应混合液中加入某些物质,下列判断错误的是( )
| A、加入KHSO4固体,v(H2)变大 |
| B、加入少量食盐水,v(H2)减小 |
| C、加入Na2CO3固体,v(H2)减小 |
| D、滴加少量CuSO4溶液,v(H2)减小 |
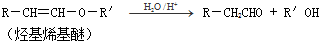
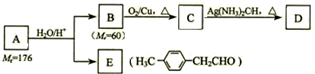
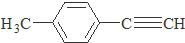 )的一条路线如下:
)的一条路线如下: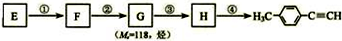
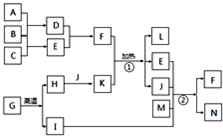 以下框图中的字母代表1-20号元素形成的常见单质及化合物,这些物质之间转化关系如图所示:其中A、B、C为单质,其余为化合物,J常温下呈液态,B在A中燃烧产生苍白色火焰,实验室常用①反应制取气体E,反应②为侯德榜制碱法的主要反应原理,L为常见的干燥剂.
以下框图中的字母代表1-20号元素形成的常见单质及化合物,这些物质之间转化关系如图所示:其中A、B、C为单质,其余为化合物,J常温下呈液态,B在A中燃烧产生苍白色火焰,实验室常用①反应制取气体E,反应②为侯德榜制碱法的主要反应原理,L为常见的干燥剂.



