题目内容
17.把ag铜铁合金粉末投入足量盐酸中,反应完全后过滤.向滤液中加入过量氢氧化钠溶液,过滤,沉淀经洗涤.干燥.灼烧,得到红棕色粉末的质量仍为ag,则此合金中铜的质量分数为( )| A. | 70% | B. | 30% | C. | 52.4% | D. | 22.2% |
分析 把ag铜铁合金粉末投入足量盐酸中,反应完全后过滤,向滤液中加入过量氢氧化钠溶液,沉淀为氢氧化铁,经洗涤、干燥、灼烧,得到红棕色粉末为氧化铁,利用组成可知氧化铁中氧元素的质量等于合金中Cu的质量,据此计算出合金中铜的质量分数.
解答 解:由铁铜合金粉末溶于足量盐酸中,加入过量NaOH 溶液,沉淀为氢氧化铁,则经洗涤、干燥、灼烧,得到红棕色粉末为氧化铁Fe2O3,
即:agFe、Cu→ag Fe2O3,
合金中Cu的质量等于氧化铁中O元素的质量,
则合金中Cu的质量分数等于氧化铁中O的质量分数,
原合金中Cu的质量分数为:$\frac{16×3}{160}$×100%=30%,
故选B.
点评 本题考查混合物反应的计算,题目难度中等,明确发生的反应找出合金与氧化物的关系是解答本题的关键,试题侧重考查学生的分析能力及化学计算能力.

练习册系列答案
相关题目
7.下列事实不能用勒夏特列原理解释的是( )
| A. | 开启啤酒瓶后,瓶中立刻泛起大量泡沫 | |
| B. | 由H2、I2蒸气、HI组成的平衡体系加压后颜色变深 | |
| C. | 在含有Fe(SCN)3的红色溶液中加入铁粉,振荡静置,溶液颜色变浅或褪去 | |
| D. | 氨水应密闭保存,置低温处 |
12.PM2.5是指大气中直径小于或等于2.5微米的颗粒物.下列说法正确的是( )
| A. | 雾天行车时,要打开车灯,这时可观察到丁达尔效应 | |
| B. | 把直径等于2.5微米的颗粒物分散到水中得到胶体 | |
| C. | 把直径小于2.5微米的颗粒物分散到水中一定得到溶液 | |
| D. | 机动车尾气排放物有SO2、NO、NO2,它们都属于酸性氧化物 |
9.下列有关物质性质的应用错误的是( )
| A. | 纯净的二氧化硅具有良好光学性能,可用于制作光导纤维 | |
| B. | 明矾能水解生成Al(OH)3胶体,可用作净水剂 | |
| C. | BaCO3难溶于水,可用作胃透视检查时的钡餐 | |
| D. | NaHCO3受热易分解,可用作焙制糕点的膨松剂 |
6.分析表中各项的排布规律,有机物X是按此规律排布的第16项,X的同分异构体共有(不考虑立体异构)( )
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| CH4 | CH2O | CH2O2 | CH4O | C2H6 | C2H4O | C2H4O2 | C2H6O |
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
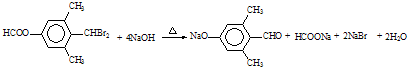
 →CH3-CHO+H2O
→CH3-CHO+H2O
 .
. .
.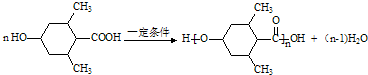 .
. (其中之一).
(其中之一).