题目内容
9.下列有关物质性质的应用错误的是( )| A. | 纯净的二氧化硅具有良好光学性能,可用于制作光导纤维 | |
| B. | 明矾能水解生成Al(OH)3胶体,可用作净水剂 | |
| C. | BaCO3难溶于水,可用作胃透视检查时的钡餐 | |
| D. | NaHCO3受热易分解,可用作焙制糕点的膨松剂 |
分析 A.光导纤维主要成分是二氧化硅;
B.铝离子水解生成氢氧化铝胶体,氢氧化铝胶体具有吸附性;
C.依据碳酸钡能够与盐酸反应生成氯化钡解答;
D.碳酸氢钠不稳定,受热分解生成二氧化碳.
解答 解:A.纯净的二氧化硅具有良好光学性能,可用于制作光导纤维,故A正确;
B.铝离子水解生成氢氧化铝胶体,氢氧化铝胶体具有吸附性,能够吸附水中杂质,故B正确;
C.碳酸钡能够与盐酸反应生成氯化钡,钡离子为重金属离子,容易引起重金属中毒,故C错误;
D.碳酸氢钠不稳定,受热分解生成二氧化碳,能够用来制作糕点的膨松剂,故D正确;
故选:C.
点评 本题考查了物质的用途,熟悉二氧化硅、明矾、碳酸钡、碳酸氢钠的性质是解题关键,题目难度不大.

练习册系列答案
相关题目
19.化学能与热能、电能等能相互转化.关于化学能与其他能量相互转化的说法错误的是( )

| A. | 化学反应中能量变化的主要原因是化学键的断裂与生成 | |
| B. | 化石燃料是不可再生能源,燃烧时将化学能转变为热能 | |
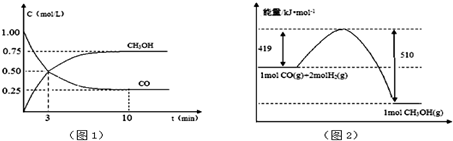
| C. | 图I所示的装置能将化学能转变为电能 | |
| D. | 图II所示的反应为吸热反应 |
20.下列各组物质可按溶解、过滤、蒸发的操作顺序,将它们分离的是( )
| A. | 氧化铜和碳粉 | B. | 硝酸钾和硝酸钠 | C. | 水和酒精 | D. | 硫酸钠和硫酸钡 |
17.把ag铜铁合金粉末投入足量盐酸中,反应完全后过滤.向滤液中加入过量氢氧化钠溶液,过滤,沉淀经洗涤.干燥.灼烧,得到红棕色粉末的质量仍为ag,则此合金中铜的质量分数为( )
| A. | 70% | B. | 30% | C. | 52.4% | D. | 22.2% |
4.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2L | |
| B. | 25℃,1.01×105 Pa,32 g O2和O3的混合气体所含原子数为2NA | |
| C. | 标准状况下,11.2LH2O 含有的分子数为0.5NA | |
| D. | 在常温常压下,44gCO2含有的分子数为3NA |
14.下列依据相关实验得出的结论正确的是( )
| A. | 在硫酸钡沉淀中加入浓碳酸钠溶液充分搅拌后,取沉淀(洗净)放入盐酸中有气泡产生,说明Ksp(BaCO3)<Ksp(BaSO4) | |
| B. | 测得Na2CO3溶液的pH大于同浓度的Na2SO3溶液,说明非金属性C<S | |
| C. | 用激光笔分别照射蛋清溶液和葡萄糖溶液,能产生光亮“通路”的是蛋清溶液 | |
| D. | 在淀粉溶液中加入稀硫酸并加热片刻再加入适量银氨溶液,水浴加热后没有银镜生成,说明淀粉没有水解 |
1.下列有关化学实验操作中“先”与“后”的说法不正确的是( )
| A. | 高锰酸钾加热制备氧气,用排水法收集满氧气后,先移出导管,后撤酒精灯 | |
| B. | 给试管加热时,先给试管来回均匀加热,后固定局部加热 | |
| C. | 大量碱液流到桌子上,先用醋酸溶液中和,后用抹布抹去 | |
| D. | 在测定溶液的pH时,先用蒸馏水湿润,后用玻璃棒蘸取溶液点在试纸中部,再与标准比色卡比较 |