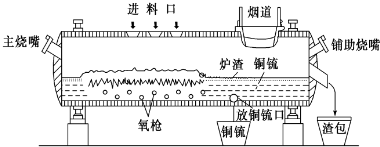
题目内容
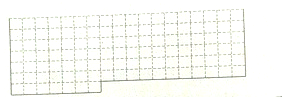
19.有aA、bB、cC、dD四种元素,原子序数均小于18,且有,d-c=c-b=b-a=5.已知A、B、C最外层电子数总和大于D最外层电子数.请根据以上情况,回答下列问题:(答题时,A、B、C、D用所对应的元素符号表示)(1)下表中实线表示元素周期表的部分边界,请先用实线不全元素周期表边界,然后把题中所述元素填入相应置.
(2)元素B的单质的结构式为N≡N,由B和D形成的化合物在工业上常用杀菌剂,写出该化合物溶于水发生反应的化学方程式NCl3+3H2O=NH3↑+3HClO.
(3)C的最高价氧化物对应的水化物与D的最高价氧化物对应的水化物之间相互反应的离子方程式可表示为Mg(OH)2+2H+=Mg2++2H2O.
(4)B的最高价氧化物对应的水化物的稀溶液与C的单质反应时,B被还原到最低价,该反应的化学方程式是4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O.
分析 aA、bB、cC、dD四种元素,原子序数均小于18,且有,d-c=c-b=b-a=5,说明四种元素原子序数依次相差5,A、B、C最外层电子数总和大于D最外层电子数,则a=2、b=7、c=12、d=17,所以A是He、B是N、C是Mg、D是Cl元素,
(1)主族元素原子核外电子层数与其周期数相等、最外层电子数与其族序数相等;
(2)B是N元素,氮气分子中N原子之间存在氮氮三键;B、D形成的化合物是NCl3,NCl3和水反应生成氨气和HClO;
(3)C的最高价氧化物对应的水化物是Mg(OH)2、D的最高价氧化物对应的水化物是HClO4,二者反应生成高氯酸镁和水;
(4)B的最高价氧化物对应的水化物的稀溶液是硝酸,稀硝酸和Mg反应时B被还原到最低价,则B元素的生成物是硝酸铵,同时镁生成硝酸镁.
解答 解:aA、bB、cC、dD四种元素,原子序数均小于18,且有,d-c=c-b=b-a=5,说明四种元素原子序数依次相差5,A、B、C最外层电子数总和大于D最外层电子数,则a=2、b=7、c=12、d=17,所以A是He、B是N、C是Mg、D是Cl元素,
(1)主族元素原子核外电子层数与其周期数相等、最外层电子数与其族序数相等,He位于第一周期0族、N元素位于第二周期第VA族、Mg元素位于第三周期第IIA族、Cl元素位于第三周期第VIIA族,其在周期表中的位置分别为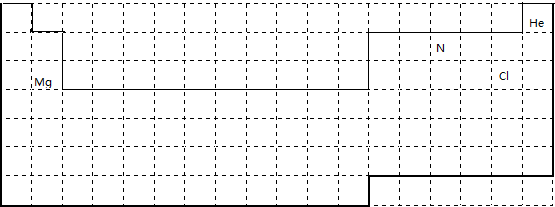 ,
,
故答案为: ;
;
(2)B是N元素,氮气分子中N原子之间存在氮氮三键,其结构式为N≡N;B、D形成的化合物是NCl3,NCl3和水反应生成氨气和HClO,反应方程式为NCl3+3H2O=NH3↑+3HClO,
故答案为:N≡N;NCl3+3H2O=NH3↑+3HClO;
(3)C的最高价氧化物对应的水化物是Mg(OH)2、D的最高价氧化物对应的水化物是HClO4,二者反应生成高氯酸镁和水,离子方程式为Mg(OH)2+2H+=Mg2++2H2O,故答案为:Mg(OH)2+2H+=Mg2++2H2O;
(4)B的最高价氧化物对应的水化物的稀溶液是硝酸,稀硝酸和Mg反应时B被还原到最低价,则B元素的生成物是硝酸铵,同时镁生成硝酸镁,化学方程式为4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O,故答案为:4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O.
点评 本题考查元素位置结构性质相互关系及应用,侧重考查周期表结构、物质性质,涉及化学方程式、离子方程式的书写,熟练掌握元素化合物知识,题目难度不大.

 一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5表示.下列有关说法正确的是( )
一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5表示.下列有关说法正确的是( )| A. | b电极为该电池的负极 | |
| B. | b电极附近溶液的pH减小 | |
| C. | a电极反应式:C6H10O5-24e-+7H2O═6CO2↑+24H+ | |
| D. | 中间室:Na+移向左室,Cl-移向右室 |
| a | b | c | d | |
| A | Cu | CuSO4 | Cu(OH)2 | Cu2O |
| B | N2 | NO2 | HNO3 | NO |
| C | CH3OH | HCHO | HCOOH | HCOOCH3 |
| D | Na | Na2O2 | NaOH | NaCl |
| A. | A | B. | B | C. | C | D. | D |
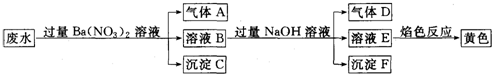
已知废水试样中可能含有下表离子中若干种.
| 阳离子 | Ba2+、K+、NH4+、Fe2+、Fe3+、X |
| 阴离子 | CO32-、SO32-、NO3-、Y |
| A. | 离子X是H+,离子Y是SO42- | |
| B. | 不能确定NO3-是否存在与废水中 | |
| C. | 沉淀C是纯净物 | |
| D. | 废水中一定存在Fe2+、NH4+,可能存在K+ |
 25℃时在10mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/LHCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示.下列说法不正确的是( )
25℃时在10mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/LHCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示.下列说法不正确的是( )| A. | 当溶液的pH=8时,溶液中NaHCO3的物质的量浓度为0.1mol/L | |
| B. | HCl溶液滴加一半时,溶液pH>7 | |
| C. | 0.1mol/LNa2CO3溶液中c(Na+)+c(H+)=c(OH-)+2c(CO32-)+c(HCO3-) | |
| D. | 在M点:c(Na+)>c(CO32-)=c(HCO3-)>c(OH-)>c(H+) |
| A. | 过氧化氢 | B. | 氯水 | C. | 硝酸锌 | D. | 氯化铜 |