题目内容
【题目】对下列药品或事故的处理正确的是( )
A.金属钠着火燃烧时用砂子灭火
B.氯水保存在无色透明的试剂瓶中
C.漂白粉保存在烧杯中
D.大量氯气泄漏时用氢氧化钠溶液浸湿的软布蒙面并迅速离开现场
【答案】A
【解析】解:A.金属钠着火燃烧时用砂子覆盖,沙子可以隔绝空气而灭火,故A正确; B.新制氯水中含有的次氯酸见光分解,所以应保存在棕色瓶中,故B错误;
C.漂白粉中含有Ca(ClO)2 , 易与空气中的水和二氧化碳反应生成不稳定的HClO,次氯酸见光易分解,应密封保存,故C错误;
D.大量氯气泄漏时用肥皂水浸湿的软布蒙面并迅速离开现场,不能用氢氧化钠溶液因为其具有强的腐蚀性,能够腐蚀皮肤,故D错误;
故选:A.

【题目】不锈钢表面用硝酸和氢氟酸的混酸处理后,产生的酸洗废液中含有Fe3+、Ni2+、NO3﹣、F﹣和+6价铬的含氧酸根离子等.如图是综合利用该酸洗废液的工艺流程: 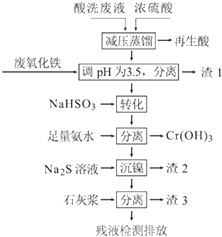
已知:
①金属离子开始沉淀和沉淀完全时的pH:
Fe3+ | Ni2+ | Cr3+ | |
开始沉淀 | 1.5 | 6.7 | 4.0 |
沉淀完全 | 3.4 | 9.5 | 6.9 |
②Ni2+与足量氨水的反应为:Ni2++6NH3[Ni(NH3)6]2+
(1)再生酸中含有 , 采取减压蒸馏的原因是 .
(2)利用废氧化铁(主要成分为Fe2O3)代替烧碱调节pH的好处是 .
(3)请写出“转化”时NaHSO3与Cr2O72﹣发生反应的离子反应方程式: .
(4)已知[Ni(NH3)6]2+为难电离的络合离子,则“沉镍”的离子方程式为: .
(5)滤渣3的主要成分为CaF2、Ca(OH)2和 .
(6)经检测,最后的残液中c(Ca2+)=0.004molL﹣1 , 则残液中F﹣浓度为mgL﹣1 , (填“符合”或“不符合”)排放标准[已知Ksp(CaF2)=4×10﹣11 mol3L﹣3 , 国家排放标准要求氟离子浓度小于10mgL﹣1].